70797-11-4
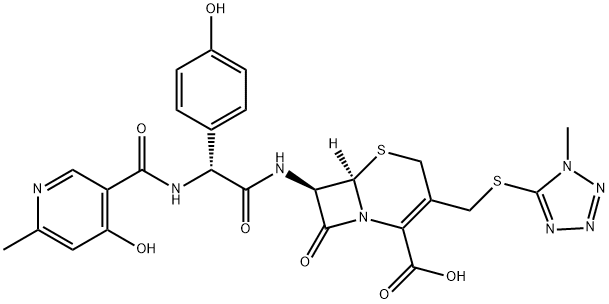 70797-11-4 结构式
70797-11-4 结构式
基本信息
头孢匹胺酸
头孢匹氨酸
头孢匹胺酸(粗)
7-[2-[(4-羟基-6-甲基吡啶-3-羰基)-氨基]-2-(4-羟基苯基)-乙酰氨基]-3-(1-甲基-1H-四唑-5-硫代甲基)-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-2-羧酸
cefpiramide acid
Suncefal:Sepatren
Cefpiramide (300 mg)
7-aMino-3-(1-Methyl-1-pyrroleane oniuM acids)Methyl-2-oxacepheMs-2-Carboxylic Acid Hydrochloride
7-[2-[(4-hydroxy-6-methylpyridine-3-carbonyl)-amino]-2-(4-hydroxy phenyl)-acetylamin]-3-(1-methyl-1H-tetrazole-5-thiomethyl)-8-keto-5-thiox-1-azole[4.2.0]octadiene-2-carboxylic acid
7-[2-[(4-hydroxy-6-methylpyridine-3-carbonyl)-amino]-2-(4-hydroxy phenyl)-acetylamin]-3-(1-methyl-1h-tetrazole-5-thiomethyl)-8-keto-5-thiox-1-azole[4.2.0]octadiene-2-carboxylic acid
5-Thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid, 7-[[(2R)-[[(4-hydroxy-6-methyl-3-pyridinyl)carbonyl]amino](4-hydroxyphenyl)acetyl]amino]-3-[[(1-methyl-1H-tetrazol-5-yl)thio]methyl]-8-oxo-, (6R,7R)-
5-Thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid, 7-[[[[(4-hydroxy-6-methyl-3-pyridinyl)carbonyl]amino](4-hydroxyphenyl)acetyl]amino]-3-[[(1-methyl-1H-tetrazol-5-yl)thio]methyl]-8-oxo-, [6R-[6α,7β(R*)]]-
(6R,7R)-7-[(2R)-2-(4-hydroxyphenyl)-2-[(6-Methyl-4-oxo-1,4-dihydropyridin-3-yl)forMaMido]acetaMido]-3-{[(1-Methyl-1H-1,2,3,4-tetrazol-5-yl)sulfanyl]Methyl}-8-oxo-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid
物理化学性质
头孢匹胺钠(Cefpiramide Sodium):C25H23N8O7S2Na。[74849-93-7]。白色至带黄白色结晶性粉末,无臭,味苦。极易溶于二甲基甲酰胺,易溶于水,微溶于甲醇,极微溶于乙醇,几不溶于氯仿、丙酮、四氢呋喃、乙腈或正己烷。
制备方法
化合物(Ⅲ)(0.2mo1)和N-甲基吗啉(0.2mo1)溶于420ml乙腈中,搅拌下冷却至-20~-15℃。加入氯甲酸异丁酯(0.2mo1),在-20~-15℃下维持10min。加入化合物(Ⅳ)(从0.42molN,O-双(三甲基硅基)乙酰胺和0.2mol化合物(Ⅳ)的游离胺在350ml乙腈中反应制得),在-15℃下搅拌2h。缓慢升至5℃,并在5℃下再搅拌1h。加入25ml甲醇,过滤除去未反应的化合物(Ⅳ)的游离胺。滤液真空浓缩至干,剩余物溶于10%碳酸氢钾水溶液。用乙酸乙酯洗2次,然后加入新鲜的乙酸乙酯,在0~5℃和搅拌下用2mol/L盐酸调至Ph=2。分出有机层,水层用乙酸乙酯提取2次。有机层合并,用氯化钠水溶液洗,无水硫酸镁干燥。减压蒸出溶剂,剩余物用二氯甲烷处理。过滤收集沉淀,用二氯甲烷洗,真空干燥,得到化合物(V),熔点127~134℃(分解)。
10mmol化合物(V)在30ml三氟乙酸的6ml苯甲醚中,在室温搅拌20min。在搅拌下,将该溶液加到400ml乙醚中。过滤收集沉淀,用乙醚洗,真空干燥,得化合物(Ⅵ),不用提纯,直接用于下步反应。
30mmol三乙胺和10mmol化合物(Ⅶ)溶于30~50ml二甲亚砜,在搅拌下加入10mmol化合物(Ⅵ),然后在室温下搅拌30min。过滤除去痕量的不溶物,在搅拌下将滤液加到600~1000ml丙酮中。过滤收集沉淀,用丙酮洗,真空干燥。然后将其溶人40~80ml水和40~80ml甲醇(或乙腈),如有不溶物,过滤除去。在5~15℃下,用2mol/L盐酸调至Ph=2。滤集沉淀,用水-甲醇(或乙腈)洗,真空干燥。最后用制备液相色谱提纯,得到头孢匹胺。
常见问题列表
头孢匹胺为半合成的第三代头孢菌素类抗生素。其体外抗菌活性与洛美沙星相仿,但半衰期明显较洛美沙星为长。该药1985年在日本上市后已广泛应用于临床治疗细菌感染,取得良好疗效,不良反应少见而轻微。本品的特点为具有广泛的抗菌谱和杀菌力,对革兰阳性菌、阴性菌及厌氧菌均有强大的抗菌活力,对β内酰胺酶相当稳定。
头孢匹胺临床主要用于敏感菌感染引起的咽喉炎、扁桃体炎、急慢性支气管炎、肺炎、肺化脓性疾病、肾盂肾炎、膀胱炎、前列腺炎、脑膜炎及妇科感染等。对革兰氏阳性菌有很强的抗菌活性、对包括革兰氏阴性菌在内的细菌亦有广谱抗菌活性。同时,对绿脓杆菌等葡萄糖非发酵革兰式阴性杆菌有很强的抗菌活性,本药的作用为杀菌,并对各种细菌产生的β-内酰胺酶稳定,用于实验性感染(小鼠)时,呈现优良的治疗效果。对青霉素类,其它头孢菌素类或氨基糖苷类抗生素耐药的细菌,尤其是对绿脓杆菌敏感。作用机制与青霉素结合蛋白(PBP)的1A,1B及3有很强的亲合性,抑制细菌细胞壁的合成,从而发挥杀菌作用。
对绿脓杆菌的最低抑菌浓度(MIC)为0.78~3.13μg/ml,对金葡菌属的MIC为0.39~0.78μg/ml,大肠杆菌的MIC为0.39μg/ml,对变形杆菌属的MIC为0.05~6.25μg/ml。对厌氧菌中消化球菌、消化链球菌的MIC80分别为0.78μg/ml和0.39μg/ml。
(1)将化合物D‑a‑(4‑羟基‑6‑甲基烟酰胺)‑P‑羟基苯基乙酸钠溶于有机溶剂中,并在‑25~‑20℃的温度下,在碱的催化下经活化剂活化,制得混合酸酐的溶液(a);
(2)将化合物7‑氨基‑3‑(1‑甲基‑1H‑四唑‑5‑硫代甲基)‑8‑氧代‑5‑硫杂‑1‑氮杂双环[4.2.0]辛‑2‑烯‑2‑羧酸(7‑TMCA)溶于有机溶剂中,并在20‑25℃的温度下加入硅烷化试剂进行硅烷化保护反应,反应完全后冷却到‑25~‑20℃得到溶液(b);
(3)将溶液(a)与溶液(b)混合,并向所得的混合溶液中加入三乙胺,在‑25~‑20℃的温度下反应完全后,加入到水溶液中并调节pH值,得到头孢匹胺。

