86639-62-5
中文名称
9-硝基喜树碱
英文名称
10-Nitrocamptothecin
CAS
86639-62-5
分子式
C20H15N3O6
分子量
393.35
MOL 文件
86639-62-5.mol
更新日期
2023/12/20 10:15:59
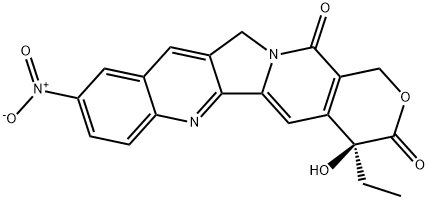 86639-62-5 结构式
86639-62-5 结构式
基本信息
中文别名
10-硝基喜树碱9-硝基喜树碱对照品
9-硝基喜树碱标准品
英文别名
RUBETICAN9-NITRO-CPT
9-Nitro-20(S)-camptothecine
CAMPTOTHECIN, 9-NITRO-20(S)-
10-Nitrocamptothecin ISO 9001:2015 REACH
4α-Ethyl-4-hydroxy-10-nitro-1H-pyrano[3',4':6,7]indolizino[1,2-b]quinoline-3,14(4H,12H)-dione
(S)-4-Ethyl-4-hydroxy-10-nitro-1H-pyrano[3',4':6,7]-indolizino[1,2-b]quinoline-3,14(4H,12H)-di
(S)-4-Ethyl-4-hydroxy-9-nitro-1H-pyrano[3',4':6,7]indolizino[1,2-b]quinoline-3,14(4H,12H)-dione
(S)-4-Ethyl-4-hydroxy-10-nitro-1H-pyrano[3',4':6,7]-indolizino[1,2-b]quinoline-3,14(4H,12H)-dione
1H-Pyrano[3',4':6,7]indolizino[1,2-b]quinoline-3,14(4H,12H)-dione, 4-ethyl-4-hydroxy-9-nitro-, (4S)-
所属类别
医药中间体:原料药中间体常见问题列表
背景及概述
喜树(Camptothecaacuminate Decne)为珙桐科喜树属植物,1985年,Hsing 等发现喜树碱及其衍生物是以 DN A 拓扑异构酶 I(Topo I)为作用靶标并抑制生物体 DN A的合成而发挥抗肿瘤的作用后,研究开发高效低毒的喜树碱抗肿瘤新药成为药学工作者的工作热点。喜树碱(Camptothecin,CPT)是由美国化学家Wall等从中国珙桐科植物喜树(Camptothecacuminata)皮果实中提取出来的一种活性物质,并确定结构为一种生物碱,它是一种具有抗肿瘤作用的中药有效成分。该类生物碱存在内酯型与羧酸盐型2种形式,具有内酯环结构的内酯型在碱性水溶液中皂化开环生成溶于水的羧酸盐型,在酸性条件下又重新环合成内酯型。但由于其对消化系统和泌尿 系统的不良反应,随后的10多年间,相关研究大大减少。直到1985年,Hisang 等揭示了喜树碱抑制拓扑异构酶I(TopoI)的新作用机制,又一次引起国内外医药界的极大重视。为寻找到低毒高效的喜树碱类似物,研究者们对喜树碱进行了多样的结构修饰,大量衍生物应运而生,有的已用于临床抗癌治疗,如拓扑替康(ropotee n)、伊立替康(irinoteean)。9-硝基喜树碱(rubitecan,9-NC)是一种新型的半合成喜树碱衍生物,又称 RFS200 0,商品名为鲁比替康(rubiteean),是美国 Super Gene公司研制的半合成喜树碱衍生物,为五环结构,含有一个吡咯[3,4-b] 喹啉环(A,B,C),一个共轭的吡啶酮环(D)和一个六元α-羟基内酯环(E),A环第9位上有一个硝基。完整的α-羟基内酯环活性的必备条件,且只有20(S)构型有活性。临床前药理学研究显示该药是非常理想的抗肿瘤药物,它不仅对常见的肿瘤均有高效的抑制作用,而且与目前常用的抗肿瘤药如5-Fu有良好的协同作用,它还能抑制亚致死损害恢复可作为肿瘤放疗的增敏剂。该药还能抑制HIV病毒的复制,未来也有望用于获得性免疫缺陷综合症AIDS的治疗。
作用机制
喜树碱及其衍生物是以拓扑异构酶I为作用靶点,抑制DN A 的合成。拓扑异构酶I是生物体内广泛存在的一类必需酶,参与DNA复制、转录、重组和修复等所有关键的过程。Topo I为单体酶,分子量为91 ku,共含有765个氨基酸,定位于第20号染色体。Topo I主要集中在DNA 活性转录区,能使 DNA的链发生断裂和再连接。在正常的酶催化循环中,Topo I与DNA 结合,DNA 的一条链断裂,形成可裂解的复合物,从而改变DNA的连环数和超螺旋数。9-硝基喜树碱以Topo I为作用靶点,其内酯环打开,酰基与Topo I中的亲核部分相互作用,与Topo I-DN A 断裂复合物可逆结合,形成药物- Topo I- DNA三元复合物,从而稳定了可裂解复合物,使复制叉不能进行下去,从而使细胞死亡。由于癌变细胞的Topo I含量很高,所以癌变细胞比正常细胞更易受 Topo I的抑制作用。细胞能否分裂决定于进入S期及M期这两个关键点,研究发现9-NC可以诱导细胞凋亡给药后细胞生长的S期和G2M期都推迟,9-NC在整个细胞周期内都有抑制并且发现这种抑制作用有剂量和时间依赖性。
药理作用
- 体外实验
用人卵巢癌SKOV-3细胞进行实验,发现9-NC可加速部分SKOV-3细胞的 凋亡,提示细胞对9-NC的敏感性存在差异;用DU145前列腺癌细胞进行实验,发现 9-NC可触发细胞凋亡的发生,且触发过程是 由CD95系统所介导的。9-NC 可使 CD95 和CD95L的表达增加,使DU145细胞从非凋亡态转变为前凋亡态,从而触发凋亡的发生。
2)放射增强作用:将 9-NC加到培养皿中对人H460肺癌细胞进行培养,之后结合放射治疗。结果显示,用l0 nmol/L 9-NC对H460细胞进行4-24h不同时间的培养,各实验组均观察到放射作用的增强,且各组间差异无显著性。另外,实验者又采用5、10、15nmol/L 9-NC对 H460细胞进行24h培养,三组的放射剂量增强率(ER)分别为1.22、1.54、2.0。
3)抗病毒作用:用已感染I型人免疫缺陷病毒(HIV-I)的U937单核细胞进行实验,结果发现9-NC可抑制病毒的复制和抑制HIV-I从被感染细胞中的释 放,且反应呈剂量依赖性。其他一些实验也证实了9-NC的抗病毒活性,如9-NC可抑制肿瘤坏死因子介导的HIV-I的激活作用,并可加速已潜在感染的T细胞凋亡;用已感染HIV-I的外周血液淋巴细胞进实验,结果同样显示 9-NC可抑制HIV-I在宿主细胞中的复制,并诱发细胞凋亡。
- 体内实验
剂量为200μg/kg/d,l周5 次,治疗后肿瘤的生长速度大大下降,有的在治疗数 周后已完全检测不到。实验显示,当9-NC 以气雾剂的形式用于治疗时,其有效剂量比以传统给药式治疗时小。若给小鼠口服上述剂量,无任何实质作用;肌注相同剂量则只有部分疗效,且十分限。
2)放射增强作用:将接种了H460 细胞的小鼠分为3组,仅口服 9-NC组(l mg/kg)、仅接受放射治疗组和口服9-NC结合放疗组。结果表明,9-NC可增 强放射治疗的效果,其增强因子(EF)为1.64。
合成路线
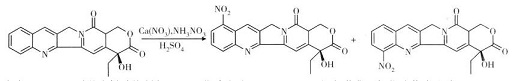
采用混合硝化剂合成20(S)-9-硝基喜树碱。以喜树碱为原料,浓硫酸为反应介质,混合硝酸盐为硝化剂进行硝化反应,再经色谱分离提纯制得目标产物9-NC。使9-NC的收率由31%上升到40%左右。研究得到的最佳工艺条件:喜树碱0.5g,浓硫酸30ml;硝酸根0.007mol,硝酸铵和硝酸钙的摩尔比为1:1;反应温度20℃,反应时间为1天。本方法具有收率高、易分离提纯等优点,具体反应过程如下:
药代动力学
已知9-NC在体内转化为9-氨基喜树碱(9-AC)。通过对小鼠、犬及人的实验测定了9-NC 转化成 9-AC的药动学参数。1)以小鼠为实验对象,单剂量口服9-NC 4.1mg /kg后Tmax为0.1h,Cmax为732ng/mL,t1/2为10.0 h,AUC为441ng/h/mL。当9-NC转化为9-AC后,9-AC 的Tmax为0.6h,Cmax为26ng/mL,t1/2为1.2 h,AUC为63ng/h/mL。
2)以犬为实验对象,单剂量口服 9-NC 1.0mg/kg后,Tmax为 0.7 h,Cmax为19.1ng/mL,t1/264h,AUC为186ng/h/mL。当9-NC转化为9-AC 后,9-AC的Tmax为2.9 h,Cmax为9.2ng/mL,t1/2为21.lh,AUC为310 ng/h/mL。
3)人体试验中单剂量口服9-NC 0.1mg/kg,Tmax为3.4 h,Cmax为483 ng/mL,AUC为2600 ng/h/mL ,t1/2为2.5h。当 9-NC转化为9-AC后,9-AC的Tmax为10.3 h,Cmax为14.0 ng/mL,AUC为3l1 ng/h/mL,t1/2为7.l h。单剂量口服9-NC 1.0mg/kg,Tmax为5.3h,达Cmax ng/mL,AUC为17194 ng/h/mL,t1/2为4.9 h。当9-NC转化为9-AC后,9-AC的Tmax为17.2 h,Cmax为208 ng/mL,AUC为9121 ng/h/mL,t1/2为13.l h。
药物相互作用
试验证实,9-硝基喜树碱与5-氟尿嘧啶(5-FU)在治疗肿瘤时具有协同作用。用HCT-8结肠癌细胞进行实验,9-NC与5-FU联用后,药物活性所加强。另外,实验中必须先给予9-NC,再给予5-FU,才能显示出二者的协同作用,提示给药 顺序是十分重要的。用接种有白血病 P-388细胞的小鼠进行实验,将9-NC与苯 丙氨酸氮芥(美法仑)联用,结果发现,两药合用后,抗癌活性有所增强,说明 9-NC与美法仑在治疗肿瘤时具有协同作用。剂型研究
- 脂质体
- 纳米粒
- 包合物
- 自微乳
- 胶束
主要参考资料
[1] 殷琦等. 正在研究中的抗肿瘤新药9-硝基喜树碱. 中国新药杂志. 2005,14(2):226-230.[2] 胡蓉蓉等. 9-硝基喜树碱研究进展. 南京中医药大学学报.2012,28(5):498-500.
[3] 郑艳等. 9-硝基喜树碱的研究进展. 化学与生物工程.200 6,23 (6):11-13.
[4] 李庆勇等. 9 - 硝基喜树碱衍生物的合成及体外抗肿瘤活性. 中国药学杂志 . 2007,42(10):786-789.
[5] 李践等. 20(S)-9-硝基喜树碱的合成研究. 医学研究杂志.2008,37(3):105-106.
[6] 闫晶超等. 9-硝基喜树碱犬体内药代动力学研究. 中国临床药理学与治疗学. 2005 ,10 (11):1220-1223.