锶标准溶液性质、用途与生产工艺
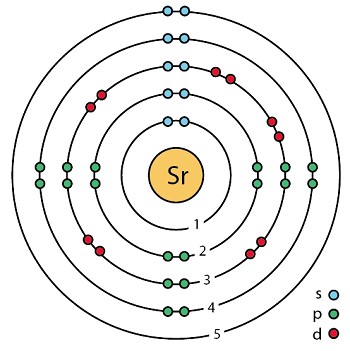
锶的符号为Sr,原子序数为38,是元素周期表第2主组的第四个成员,锶是典型的碱土元素。电子结构是带有两个额外的外部5s电子的结构。锶是一种碱土金属,是一种柔软的银白色或微黄色金属元素,具有很高的化学反应性。由于其与氧气和水的极强反应性,该元素仅在与其他元素的化合物中自然存在。暴露在空气中,金属会变成黄色。同位素90Sr存在于放射性尘埃中,半衰期为28.90年。锶通常存在于自然界中,是地球上含量最高的第15个元素,在所有火成岩中平均占0.034%。主要以硫酸盐矿物天青石(SrSO4)和碳酸盐锶矿(SrCO3)的形式发现。
锶和锶矿都以苏格兰的一个村庄命名,从这附近的铅矿开采的矿石中首次发现了矿物。 1787年,一种有趣的矿物从一个铅矿来到爱丁堡,该矿位于苏格兰西部高地阿盖尔湖苏纳特湖岸上的一个小村庄里。当时,该物质被认为是某种钡化合物。三年后,斯科特(Scott)的爱尔兰化学家阿黛尔·克劳福德(Adair Crawford)发表了一篇论文,声称该矿物拥有一个包括新化学元素的新物种。其他化学家后来用这种元素制备了许多化合物,并指出它导致蜡烛的火焰燃烧成红色,而钡化合物则发出绿色。格拉斯哥大学的另一位医学教授托马斯·霍普(Thomas Hope)在1793年将这种新矿物命名为锶锶。汉弗莱·戴维(Humphrey Davy)在研究各种含有熔融氯化物(如SrCl2和氧化汞)的碱土的电解过程中,最终于1808年将其分离。 1808年6月30日,他在皇家学会的一次演讲中宣布了他的工作。为了与其他碱土的命名保持一致,他将其更名为锶。
自然界中没有发现锶金属。 它的盐和氧化物只占地壳的0.025%。锶有29种同位素,范围从Sr-75到Sr-102。 锶的四种天然形式是稳定的而不是放射性的。 这些稳定的同位素是Sr-84,占地球上元素的0.56%; Sr-86,占9.86%; Sr-87,占总数的7.00%; Sr-88,占地球上锶的82.58%。 其余的同位素具有放射性,半衰期范围从几微秒到数分钟,数小时,数天或数年。 大多数(但不是全部)是在核反应堆或核爆炸中产生的。 两个重要的放射性同位素是Sr-89和Sr-90。

锶的两种主要矿物是碳酸盐,锶锶矿SrCO3和硫酸盐含量更高的天青石SrSO4。 由于大多数应用都涉及钙和钡,因此元素锶仅具有很小的用途。 锶合金用作真空管的“吸气剂”。 它被掺入玻璃中以制造彩色电视机的显像管。 锶化合物用于示踪弹和烟花中,产生红色信号弹。 钛酸锶是宝石。 半衰期为29年的放射性锶90是高能β发射体。 它是核裂变的产物。 这种同位素是航天器和远程气象站中的一种轻型核动力源。
锶是在墨西哥和西班牙的锶矿(SrCO3)和天青石(SrSO4)的矿石中发现的。 这些矿石用盐酸(HCl)处理后,会生成氯化锶(SrCl2),然后与氯化钾(KCl)一起形成共晶混合物以降低SrCl2的熔点,作为石墨中的熔融电解质碟形电解装置。 此过程产生的Sr阳离子在阴极收集,在那里它们获取电子以形成锶金属。 同时,Cl-离子在阳极释放电子,并以氯气Cl2的形式释放出来。
锶金属可能以粉末形式自发爆炸。金属锶及其某些化合物在加热时都会爆炸。如果用锤子敲打,某些化合物会爆炸。 金属锶及其某些化合物都会与水反应生成氢氧化锶[Sr(OH)2]并释放出氢气。放热反应产生的热量可能导致氢燃烧或爆炸。
[Sr + 2H2O→Sr(OH)2 + H2↑]
某些化合物,例如铬酸锶和氟化锶,是致癌物,如果摄入会中毒。锶90特别危险,因为它是放射性骨搜寻者,可替代骨骼组织中的钙。暴露于过量Sr-90的人群中可能发生辐射中毒和死亡。距爆炸源很远的地方,动植物可能会吸入90锶以及通过核武器爆炸产生的某些其他放射性同位素,然后进行大气运输。这一因素和其他因素导致禁止对核武器和热核武器进行大气测试。
锶粉末遇火易造成着火和爆炸危害。加热至熔点以上也能自燃。因为锶与水反应释出氢;当金属锶贮存在潮湿的情况下,就有可能有气体爆炸的危险。也容易与卤素和磷反应。遇酸类会剧烈反应而释放出氢气。
锶的毒性介于钙和钡之间。误服可引起胃肠道症状,肢体痛性抽搐,少数病例可累及心肌。放射性的89锶和90锶则有很高的毒性,动物腹腔内注射金属锶的LD
50:88~247 mg/kg。要使患者脱离污染区,安置休息并保暖。不慎溅人眼睛要用大量水冲洗15 min,严重者就医诊治。皮肤接触先用水冲洗,再用肥皂彻底洗涤,如有灼伤就医诊治。误服立即漱口,急送医院救治。
化学性质
银白色柔软金属。相对密度2.63。熔点769℃。沸点1384℃。面心立方。化学性质居于钙与钡之间,活泼性强,在空气中迅速被氧化,表面形成黄色氧化膜。在空气中粉碎时可自燃。加热能与氢结合形成氢化锶。也容易与卤族元素和磷反应。电阻率(20℃)23μΩ?cm,熔化热7.43kJ/mol;汽化热136.9 kJ/tool。电负性1.10。遇水即分解释出氢及大量热,使氢引起燃烧,发出深红色火焰。溶于酸类并产生氢气引起燃烧,溶于醇。
用途
用于合金,真空管的吸气剂。
用途
用于制造合金,及用作电子管的吸气剂,也用于化学分析、制烟气等。
生产方法
铝热还原法先将硝酸锶热分解制得氧化锶,用细粒铝作还原剂,配料比按3SrO:2AI进行,把氧化锶和铝先制成团矿,将此团矿装入钢制蒸馏器进行真空脱气处理,其处理温度为90℃,真空度最终应为10mmHg。将薄铁板制内筒按蒸馏器整个放人,在1150℃进行12h还原反应,得到锶沉积物纯度为99%。将蒸馏器降至500℃以下,再将内简取出切开后剥离沉积物,制得金属锶成品。
锶标准溶液
上下游产品信息
上游原料
下游产品