39450-01-6
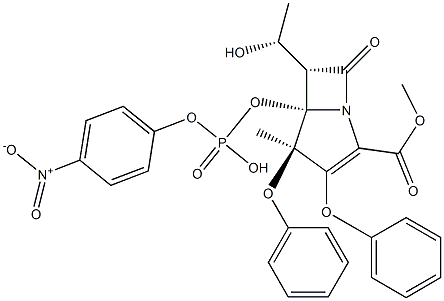 39450-01-6 结构式
39450-01-6 结构式
基本信息
重组蛋白酶K
蛋白激酶K溶液
ML蛋白酶K溶液
蛋白酶K(原装)
蛋白酶K(进分)
蛋白酶K(SIGMA)
20MG/ML蛋白酶K溶液
蛋白酶K 来源于林伯氏白色念球菌
蛋白酶K溶液(20 MG/ML)
20mg
40U/MG
CHLOROM
3.4.21.14
Protease K
KProteinas
PROTEINASE K
EC 3.4.21.64
EC 3.4.21.14
物理化学性质
应用领域
常见问题列表
蛋白酶K是一种从白色念珠菌分离出来的强力蛋白溶解酶,具有很高的比活性,是DNA提取的关键试剂。该酶在较广的pH范围(4?12.5)内及高温 (50?70°C)均有活性,用于质粒或基因组 DNA、RNA的分离。
蛋白酶K能消化天然的角蛋白(Kerati),而得名蛋白酶K。其主要的切割位点是脂肪族氨基酸和芳香族氨基酸的羧基端肽键。由于其广泛地的切割能力,在实验室中很常用。此蛋白酶属于丝氨酸蛋白酶SB超家族中的S8家族(枯草杆菌蛋白酶也属于这个超家族)。蛋白酶K的分子量为28.9千道尔顿。
蛋白酶K的酶活力,>30U/mg。在37℃,以血红蛋白为底物,1分钟内可以产生相当于1微摩尔酪氨酸Folin阳性的氨基酸或多肽的蛋白酶K的量,定义为一个单位蛋白酶K酶活力。 在很宽的pH范围内有效,有效的pH范围为pH4.0-12.5,最佳pH范围为pH7.5-8.0。 蛋白酶K的最佳反应温度为65℃,但在65℃或更高的温度蛋白酶K自身的也非常迅速地降解。很多时候反应温度选择50 -55℃。
蛋白酶K时常应用于分子生物学领域。在制备核酸时,蛋白酶K可以将杂蛋白去除,并迅速使核酸酶失活,避免其降解目标产物DNA和RNA。另外,蛋白酶K还有其他优点,它在变性剂存在下仍能保有活性,如SDS、尿素、EDTA等等,这点与其他蛋白酶(如胰蛋白酶、胰凝乳蛋白酶)相当不同。
蛋白酶K由于能够消化角蛋白(kratin)因此被命名为蛋白酶K。蛋白酶K家族包含了各种由真菌、酵母及革兰氏阴性细菌分泌的细胞内肽酶,其中细菌分泌的酶有高度的序列相似性(>55%)。林伯氏白色念球菌(Tritirachiumalbum Limber)分泌产生蛋白酶K是该家族的模式蛋白。蛋白酶K对大多数底物均有切割活性,但是偏好于带有脂肪族及芳香烃的肽链。其属于丝氨酸蛋白酶,拥有典型的丝氨酸活性位点:Asp39–His69–Ser224 。其含有一个单练肽链包含277氨基酸位点,并拥有2个二硫键和一个空置的半胱氨酸位点以及两个钙离子结合位点。
蛋白酶K的应用主要为核酸提取时去除DNA酶和RNA酶,并且可将结合于基因组上的组蛋白去除,还可用于碱性磷酸酶的失活。目前分子生物学技术已应用于许多检测标准中,例如转基因检测、动物属性检测、致病微生物检测等。在分子生物学检测中核酸的提取质量直接影响了后续PCR反应的扩增效率。许多标准在核酸提取步骤中都设立了添加蛋白酶K消化的步骤,以期提取较纯的核酸。为了保护核酸,分子生物学核酸提取实验中通常含有EDTA等试剂,由于EDTA可以与金属离子络合,因此可能会导致酶活性受到影响;并且通常为pH8.0时和55℃条件下进行消化,不同pH值和温度条件会使得酶活性受到影响。
