13569-63-6
中文名称
三氯化铼
英文名称
RHENIUM(III) CHLORIDE
CAS
13569-63-6
分子式
Cl3Re
分子量
292.57
MOL 文件
13569-63-6.mol
更新日期
2023/03/20 19:41:20
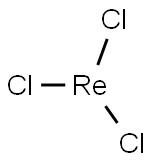 13569-63-6 结构式
13569-63-6 结构式
基本信息
中文别名
三氯化铼氯化铼(III)
三氯化铼(III)
英文别名
Einecs 236-987-1RHENIUM CHLORIDE
RHENIUM(+3)CHLORIDE
RHENIUM TRICHLORIDE
RHENIUM(III) CHLORIDE
Trichlororhenium(III)
rheniumchloride(recl3)
Rhenium(III) trichloride
Rheniumchloridemeshredblackpowder
Rhenium(III) chloride, 99.8+% (metals basis)
所属类别
无机化工:金属氯化物及盐物理化学性质
外观性状深红色六方系晶体。沸点高于550℃。溶于水、酸、 碱、液氨及醇,微溶于醚。稀释其水溶液时,可析出三氧化铼的水合物。新制备的水溶液与硝酸银不反应。湿空气中放置2~3小时生成二水合物,后者在五氧化二磷上干燥可失去水分。常以二聚体的形式存在。
熔点decomposes at 500℃ [LID94]
沸点>550°C
密度4.810
溶解度H2O:微溶(lit.)
形态粉末
颜色深红
水溶解性易溶于水。
敏感性湿气敏感
晶系Three sides
空间群R3m
晶格常数
| a/nm | b/nm | c/nm | α/o | β/o | γ/o | V/nm3 |
| 1.021 | 1.021 | 2.035 | 90 | 90 | 120 | 1.8361 |
CAS 数据库13569-63-6
安全数据
警示词警告
危险性描述H315-H319-H335
危险品标志Xi
危险类别码36/37/38
安全说明26-37/39
WGK Germany3
RTECS号VI0875000
TSCAYes
毒性cat,LDLo,intravenous,20mg/kg (20mg/kg),VASCULAR: BP ELEVATION NOT CHARACTERIZED IN AUTONOMIC SECTION,Journal of Pharmaceutical Sciences. Vol. 57, Pg. 321, 1968.
制备方法
方法1
三氯化铼(Ⅲ)是利用五氯化铼在氮气中的热分解来制备的。将一支硬质玻璃燃烧管做成与制备五氯化铼所用燃烧管相同的多球管子(见图1)。照条目的方法制备五氯化铼并使其升华进入球D中。停止通氯气,并用氮气置换,当氯气已排净时,在流速较大的氮气流中小心地给五氯化铼加热。使一部分升华到下一个球中,剩下的残渣是三氯化铼。当不再有棕色的烟产生时,五氯化铼即已完全分解。剩余的三氯化物要在很高的温度下才能升华,其气态是绿色的。要特别小心勿使三氯化物过热,若在常压下利用升华来提纯三氯化铼将会导致强烈的分解。在球管中留下的五氯化铼可以用同法使之转化。捕集瓶中往往会有少量的铼,但大部分铼会留在后面成为粗制的三氯化铼。燃烧管已冷却后,可将燃烧舟取出,轻敲燃烧管将三氯化铼取出,产率约为70%。图1:五氯化铼是利用金属铼在干燥氯气中的直接燃烧作用来制备的。2Re+5Cl2→2ReCl5
如果需要制备纯净的产物,在全部五氯化铼都已分解后,将燃烧管在第一个凹缩处熔封起来。将产物摇到球D中,将管子成45°倾斜放置,并在减压下、450℃时使三氯化铼升华。在管子进入管式电炉处放一块石棉隔板将能使三氯化物恰好在电炉的边缘上凝聚。将产物升华两次,冷却至室温,并恰在生成三氯化铼处的前后两点将管子截断。可以将暗红色的晶状物弄碎,移入一只称量瓶、放在干燥器中储存而不必担心它会发生分解。应避免日光的直接照射,否则会生成氯氧化物。产率一般约为60%至65%。
常见问题列表
理化性质
三氯化铼,化学式ReCl3。分子量292.57。一种暗红色或紫色晶体。熔点727℃。沸点800~850℃。500℃真空升华,蒸气为绿色。溶于水、酸、碱、液氨及乙醇,稍溶于乙醚。水溶液呈红色,不能使硝酸银溶液迅速沉淀出氯化银。可被乙醚萃取。缓慢水解而析出水合氧化铼Re2O3·xH2O,但在盐酸水溶液中却很稳定。在常温下不被高锰酸钾或氯水所氧化。经升华制得的为三聚体(ReCl3)3,是簇状化合物。在250~300℃条件下被氢气还原为金属铼。在氧气中加热生成四氯一氧化铼及一氯三氧化铼。由氮气中热分解五氯化铼制得。
自然资源
铼本身无独立矿床,常分散在其他有色金属矿体中,主要和辉钼矿伴生共存,多以微量伴生于钼、铜、铅、锌、铂、铌等矿物中。
制备
一种三氯化铼制备方法:将铼粉均匀填装于气氛炉中,厚度保持在2cm,先将炉温升至100℃,保持2h后,通入氯气,控制气体流量1m3/h,然后,以20℃/min的升温速率,缓慢升温至300℃,反应10h,自然冷却,待温度降低至200℃时,停止通入氯气,改为通入氮气,控制氮气的气体流量为3m3/h,反应3h,自然冷却至室温,得暗红色的晶状物,经X射线衍射检测分析,产物为三氯化铼,产率为85%。由氮气中热分解五氯化铼制得:ReCl5 → ReCl3 + Cl2。应避免日光直接照射,否则会生成氯氧化物。产率一般约为60%至65%。
