纳米氧化铪粉性质、用途与生产工艺
氧化铪(HfO2)是白色晶体粉末。纯氧化铪以三种形式存在,一种是无定型状态,另外两种为晶体。在<400℃煅烧氢氧化铪、氧氯化铪等不稳定的化合物时,可以得到无定型氧化铪。将其氧化铪继续加热至450~480℃,开始转化为单斜晶体,继续加热至1000~1650℃发生晶格常数逐步增加的趋势,并转化为4个氧化铪分子的单体。当1700~1865℃时开始转化为四方晶系。
向氧化铪中添加少量氧化镁、氧化钙、氧化锰等氧化铪,在1500℃以上可以形成面心立方晶格的固溶体。如向氧化铪中加8% ~ 20%氧化钙,则晶格常数α相应从0.5082nm增加至0.5098nm。若添加的量达到形成CaHfO3时,则晶体结构转化为菱形晶系。 单斜晶体氧化铪的密度为9.68g/cm3,熔点3031K,沸点5673K。
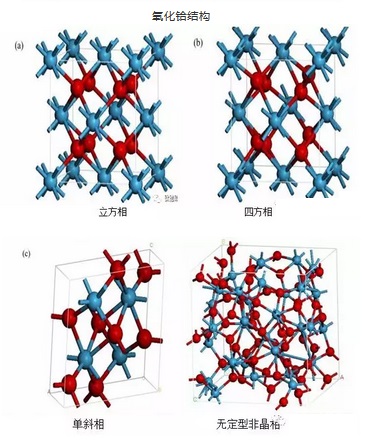
氧化铪结构1
氧化铪的化学性质与氧化锆相似,其活性与煅烧温度有关,煅烧温度越高,化学活性性越低。无定型氧化铪容易溶解于酸中,但是结晶型氧化铪即使是在热盐酸或者是硝酸中也不发生反应,而仅溶于热浓的氢氟酸和硫酸中。结晶型氧化铪与碱和盐酸溶后,则容易稀酸中。在1100℃下,氧化铪与铪酸锂。在高于1500℃氧化铪与碱土金属氧化铪与二氧化硅等作用,生成铪酸盐和硅酸铪。在1800℃以上与氧化硅组成一系列的固溶体。
铪盐水解可以得到两性的氢氧化铪,氢氧化铪在100℃下干燥能够达到HfO(OH)2,再升高温度即转换为氧化铪。
在碳化过程中可有Hf2O3与HfO形成,但是对此研究较少。
二氧化铪为白色或灰色粉末。不溶于水、盐酸和硝酸和其他一般无机酸,在氢氟酸中缓慢溶解生成氟铪酸盐。与热浓硫酸或硫酸氢盐作用生成硫酸铪。与碳在氯气存在下混合加热得到四氯化铪。与氟硅酸钾作用生成氟铪酸钾。
氧化铪为白色立方晶体,比重9.68。熔点2,758±25℃。沸点约5,400℃。单斜晶系的二氧化铪在1,475~1,600℃足量氧气氛中转化为四方晶系。不溶于水和一般无机酸,但在氢氟酸中缓慢溶解。
与热的浓硫酸或酸式硫酸盐作用形成硫酸铪[Hf(SO4)2],与碳混合后加热通氯生成四氯化铪(HfCl4),与氟硅酸钾作用生成氟铪酸钾(K2HfF6),与碳在1,500℃以上作用形成碳化铪HfC。
氧化铪可由铪的碳化物、四氯化物、硫化物、硼化物、氮化物或水合氧化物直接高温灼烧制取。
氧化铪(HfO2)为锆铪分离的产物,目前只有美、法等国家在生产核级锆时产生有氧化铪。中国早期就已经具备生产核级 Zr,并生产少量氧化铪的能力。但是产品数量稀少,价格昂贵。作为铪的主要化学产品,通常用作光学镀膜材料,很少量开始试用于高效集成电路,氧化铪在高端领域的应用尚待开发。
氧化铪在光学镀膜领域的应用 HfO2的熔点比较高、同时铪原子的吸收截面较大,捕获中子的能力强,化学性质特别稳定,因此在原子能工业中具有非常大应用的价值。自上世纪以来,光学镀膜得到了很快的发展,HfO2在光学方面的特性已经越来越适应光学镀膜技术的要求,所以 HfO2在镀膜领域的应用也越来越广泛,特别是它对光有比较宽的透明波段,在光透过氧化铪薄膜时,对光的吸收少,大部分通过折射透过薄膜,因此HfO2在光学镀膜领域的应用越来越被重视。
二氧化铪(HfO2)是一种具有较高介电常数的氧化物。作为一种介电材料,因其较高的介电常数值(~ 20),较大的禁带宽度(~ 5.5 eV),以及在硅基底上良好的稳定性,HfO2被认为是替代场效应晶体管中传统 SiO2 介电层的理想材料。如果互补金属氧化物半导体器件尺寸低于 1 μm,以二氧化硅为传统栅介质的技术会带来芯片的发热量增加、多晶硅损耗等一系列问题,随着晶体管的尺寸缩小,二氧化硅介质要求必须越来越薄,但是漏电流的数值会因为量子效应的影响随着二氧化硅介质厚度的较小而急剧升高,所以急需一种更可行的物质来取代二氧化硅作为栅介质。
二氧化铪是一种具有宽带隙和高介电常数的陶瓷材料,近来在工业界特别是微电子领域被引起极度的关注,由于它很可能替代目前硅基集成电路的核心器件金属氧化物半导体场效应管(MOSFET)的栅极绝缘层二氧化硅(SiO2),以解决目前MOSFET中传统SiO2/Si结构的发展的尺寸极限问题。
用途
为生产金属铪和铪合金的原料。用作耐火材料、抗放射性涂料和催化剂。
生产方法
当加热到高温时铪与氧直接化合生成氧化铪。也可通过其硫酸盐或草酸盐经灼烧而得。
纳米氧化铪粉
上下游产品信息
上游原料
下游产品