背景及概述[1]
(R)-2,5-二氢-3,6-二甲氧基-2-异丙基吡嗪可作为医药合成中间体,可由D-缬氨酸为反应原料,制备N-(叔丁氧羰基)-D-缬氨酸,进一步反应生成中间体N-(叔丁氧羰基)-D-甘氨酸乙酸甲酯,最后与四氟硼酸三甲基氧鎓反应制备得(R)-2,5-二氢-3,6-二甲氧基-2-异丙基吡嗪。
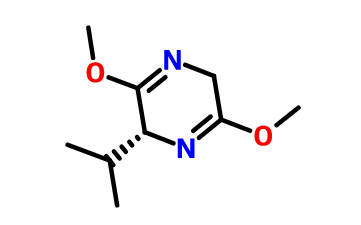
制备[1]
步骤1:N-(叔丁氧羰基)-D-缬氨酸的制备
将NaHCO3(717g,8.53mol)加入到D-缬氨酸(500g,4.27mol)的水(6.4L)溶液中,然后加入碳酸氢二叔丁酯(932g)的THF溶液(6.4公升)。将混合物搅拌并在回流下加热16小时,在真空下浓缩以除去THF。加入EtOAc(4.5L),并将混合物冷却至10℃,然后用饱和NaHSO4水溶液(3.3L)调节至pH3。分离各层,并将水层用EtOAc(4L)萃取。用水(2L)和盐水(2L)洗涤合并的EtOAc层,用MgSO4干燥,并在真空下浓缩,得到N-(叔丁氧羰基)-D-缬氨酸(924g,99%)。
步骤2:N-(叔丁氧羰基)-D-甘氨酸乙酸甲酯的制备
在5分钟内,在30分钟内将氯甲酸异丁酯(580g,4.25mol)添加到N-(叔丁氧羰基)-D-缬氨酸(924g,4.25mol)和Et3N(430g,4.25mol)的CH2Cl2(12.3L)混合物中。加完后,将混合物在0-5℃下搅拌30分钟。在另一个烧瓶中,将甘氨酸甲酯盐酸盐(534g,4.25mol),Et3N(430g,4.25mol)和CH2Cl2(12.3L)的混合物搅拌30分钟,然后添加N-(叔丁氧羰基)-D-缬氨酸。添加完成后,将混合物在室温搅拌16小时,然后用水(3×15L)和盐水(5L)洗涤,干燥,并真空浓缩,得到N-(叔丁氧羰基)-D-甘氨酸乙酸甲酯(1118g,91%)。
步骤3:(2R)-异丙基哌嗪-3,6-二酮的制备
将N-(叔丁氧羰基)-D-甘氨酸乙酸甲酯(999g,3.46mol)的1,2-二氯苯(9L)溶液在175-180℃下加热18h,通过蒸馏除去形成的MeOH。在大气压下借助氮气流通过蒸馏除去6L溶剂后,将混合物冷却至50℃,并小心地添加MTBE(5L)。将混合物冷却至室温并过滤。将得到的固体用MTBE(200mL)洗涤,并在100℃下真空干燥,得到(2R)-异丙基哌嗪-3,6-二酮(372g,69%)。1HNMR(DMSO-d6):δ0.84(d,3H,J=6.8Hz),0.91(d,3H,J=6.8Hz),2.10(m,1H),3.51(m,1H),3.61和3.81(AB,2H,J=17.7Hz),8.01(s,1H),8.20(s,1H)。
步骤4:(R)-2,5-二氢-3,6-二甲氧基-2-异丙基吡嗪的制备
在室温下,向(2R)-异丙基哌嗪-3,6-二酮(135g,0.86mol)和四氟硼酸三甲基氧鎓(450g,3.07mol)的混合物中加入CH2Cl2(2L)。将混合物在室温搅拌84小时。通过在氮气下过滤收集所得固体,并用CH2Cl2(300mL)洗涤。将固体分批添加到4°C的NaHCO3饱和水溶液(3L)和CH2Cl2(2L)剧烈搅拌的混合物中,同时根据需要通过同时添加3MNaOH水溶液将pH保持在8至9之间。分离混合物,并将水相用CH2Cl2(2×500mL)萃取。合并的有机相用盐水(500mL)洗涤,干燥,并在真空下浓缩。通过真空蒸馏(沸点72℃/4.5Torr)纯化浅黄色残余油(93%,通过GC-MS纯化),得到(R)-2,5-二氢-3,6-二甲氧基-2-异丙基吡嗪(134.6g,85%,96%ee),为无色油。1HNMR(CDCl3):δ0.77(d,3H,J=6.8Hz),1.04(d,3H,J=6.8Hz),2.33(m,1H),3.69(s,3H),3.73(s,3H),3.90(m,3H).13CNMR(CDCl3):δ17.25,19.30,32.70,46.88,52.66,52.71,61.34,162.60,165.09.MS:m/z184(M+).
参考文献
[1] Chen J , Corbin S P , Holman N J . An Improved Large Scale Synthesis of the Schöllkopf Chiral Auxiliaries: (2 R )- and (2 S ) - 2,5Dihydro3,6-dimethoxy-2-isopropylpyrazine[J]. Organic Process Research & Development, 2016, 9(2):185-187.
