性状
本品为类白色粉末,其水合物为粉红色至浅褐色固体粉末,微溶于乙醇、甲醇、乙睛、乙酸乙酯,几乎不溶于水。
制剂规格
片剂:40mg
用法与用量
推荐剂量:口服, 160mg/d,每天1次,用药3周,停药1周,4周为1周期。与低脂早餐共服。
生产厂家
Q德国拜耳医药公司
类别
抗肿瘤药;新型口服多靶点磷酸激酶抑制剂
研制单位
Bayer医疗保健制药公司和Onyx制药有限公司
上市时间
2012年9月,转移性结直肠癌;2013年2月,进展期胃肠间质瘤
作用机制 【1】
体外和体内临床前研究显示,本品具有广泛的抗肿瘤活性。作为多靶点的激酶抑制剂。其靶向作用涉及肿瘤血管生成和肿瘤细胞增殖的多个蛋白激酶,这些激酶包括:
①与肿瘤血管生成相关的血管内皮生长因子受体.1(vasctllar endothelial growth fac.for receptor—l,VEGFR—1)、VEGFR一2、VEGFR—3、酪氨酸蛋白激酶受体-2(Tie-2);
②与肿瘤细胞增殖相关的原癌基因c.Kit、酪氨酸蛋白激酶受体RET、原癌基因c—RAF、丝氨酸/苏氨酸蛋白激酶B(BRAF)、丝裂原激活的蛋白(mitogen—activated protein,MAP)激酶p38:
③与肿瘤微环境相关的血小板衍生生长因子受体.13(platelet derived growth fac.tor receptor一13,PDGFR一13)、成纤维细胞生长因子受体一1(fibroblast growth factor receptor.1,FGFR.1)。本品通过阻断和抑制上述激酶的活性.发挥阻断肿瘤血管生成和抑制肿瘤细胞增殖的多重抗肿瘤作用。
本品与索拉非尼结构相似.区别仅为本品的中央苯环上增加了一个氟原子,这使得两个药物既相似又有着不同的生化特性。体外生化分析显示,相对于索拉非尼,本品对VEGFR-2、PDGFR—B、FGFR一1和c.Kit的抑制作用更强。
同时,本品还能抑制Tie-2,具有更广泛的抗血管生成作用。在抑制肿瘤细胞增殖方面.本品和索拉非尼均靶向c.RAF、野生型BRAF和BRAF-600.并干扰肿瘤发生时异常激活的MAP激酶胞内信号传导通路。其中,抑制MAP激酶p38是本品独有的特征。由此可见,与索拉非尼相比,本品靶向的激酶范围更广.在药理学上具有更强的作用,是一个颇有前景的抗肿瘤药物。
药代动力学【1】
单剂量13服本品160mg后T1/2为4h,平均AUC为70.4p.g·h/nll。本品达到稳态时,平均AUC为58.31.Lg·h/ml。AUC的个体间变异率为35%~44%,平均相对生物利用度为69%~83%。本品体内代谢经肝肠循环.由CYP3A4和UGTIA9参与.主要代谢产物为M2(N.氧化代谢物)和M5( N-氧化和N-去甲基代谢物) ,在体外表现出与原型药物相似的药理学活性和稳态浓度。
药物相互作用
避免与强CYP3A4诱导剂或强CYP3A4抑制剂同时使用。
适应证
本品作为一种激酶抑制剂,适用于既往曾使用氟嘧啶、奥沙利铂和伊立替康进行抗-VECF治疗或抗ECFR治疗的转移性结直肠癌( CRC)。
不良反应【1】
最常见不良反应(≥30% )是乏力/疲乏、食欲减低和食物摄人量、手足皮肤反应(HFSR)[掌足红肿( PPE)]、腹泻、口腔黏膜炎、体重减轻感染、高血压和发音困难。早期临床试验观察到本品最常见的不良反应是皮肤毒性(手足皮肤反应、皮疹脱屑、脱发)、疲劳、高血压、黏膜炎、腹泻和甲状腺功能障碍,与其他类似的口服多靶点激酶抑制剂的不良反应相似。
大多数不良反应为轻、中度,可以经过临床处理得到控制。对于转移性结直肠癌患者,COR-RECT试验显示的本品组和安慰剂组治疗相关不良反应的发生率分别为93%和61%。本品相关的最常见3级及以上不良反应为手足皮肤反应(17%)、疲劳(9% )、腹泻(7%)、高血压(7% )和皮疹或脱屑(6%),与早期临宋试验结果相似。
此外,Grothey等分析了CORRECT试验中本品不良反应发生的时间特征,3级及以上不良事件手足皮肤反应疲劳、 高血压和皮疹或脱屑的发生率在治疗第1周期达到高峰,之后发生率逐渐降低至相对稳定的低水平状态。腹泻的发生率在整个治疗期间相对恒定。该分析结果显示,本品治疗最为常见的不良反应通常发生在治疗的早期,因此早期应密切监测不良反应。对于GIST患者,GRID研究显示,本品组和安慰剂组治疗相关不良反应的发生率分别为98%和68%。本品相关的最常见3.4级不良反应为高血压(23%)、手足皮肤反应(20% )和腹泻(5% ),可通过调整剂量进行处理。
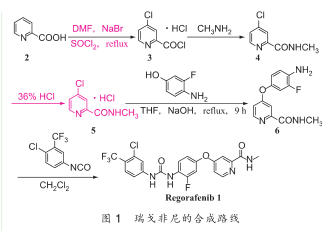
合成路线【2】
参考文献
[1]邹栩,陈玲主编;顾凯,王卉,郝静梅副主编,世界上市新药动态与分析,中国医药科技出版社,2016.06,第143页
[2]苏鹏,袁晨欢,王德才,高瑞,赵伟.瑞戈非尼的合成工艺改进的研究[J].药学与临床研究,2015,23(04):368-369.
