基本描述
4-氯-3-氟苯甲酸的CAS号是403-17-8,分子式是C7H4ClFO2,分子量为174.56。熔点是190-192°C,沸点是290.9±20.0°C(Predicted),密度是1.477±0.06g/cm3(Predicted)以及酸度系数(pKa)是3.63±0.10(Predicted)。4-氯-3-氟苯甲酸易溶于甲醇和二甲基亚砜。4-氯-3-氟苯甲酸是一种重要的精细化工中间体,可用于医药产品、生物工程、活性染料、聚酯化合物及农药等的合成[1-2]。
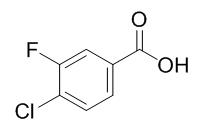
图1 4-氯-3-氟苯甲酸的结构式。
合成

图2 4-氯-3-氟苯甲酸的合成路线[3]。
将亚氯酸钠(17g)在冰冷却下分批加入到由4-氯-3-氟苯甲醛(10g)、氨基磺酸(18g)、叔丁醇(50ml)和水(50ml组成的混合溶液中,并将混合物搅拌4天,同时将系统温度逐渐升高至室温。用乙酸乙酯稀释反应混合物,用水、1N盐酸和饱和氯化钠水溶液洗涤。用无水硫酸钠干燥所得有机层,减压蒸馏出溶剂后,将所得残余物从二异丙醚和己烷的混合溶剂中重结晶,得到标题化合物4-氯-3-氟苯甲酸(11.2g)。1H-NMR(DMSO-D6)δ:7.72(1H,dt,J=8.3,1.5Hz),7.77(1H、dt,J=8.2,1.6Hz),7.82(1H,dt、J=9.7,1.5 Hz),13.45(1H,s)。合成路线图如图2所示。
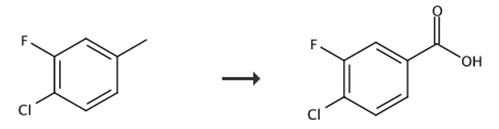
图3 4-氯-3-氟苯甲酸的合成路线[4]。
在O2气氛下,将反应物(0.1mmol,9.2mg)、CeCl3(5mol%,1.2mg),CCl3CH2OH(20mol%,20μL(1M CH3CN溶液))、CH3CN(2ml)添加到带有搅拌棒的25ml石英玻璃管中。将管垂直于400 nm LED灯(10 W)。在60°C下,在蓝光照射下搅拌混合物48小时。如薄层色谱所示,反应完成。加入乙酸乙酯和水提取三次。减压浓缩有机相得到4-氯-3-氟苯甲酸。合成路线图如图3所示。
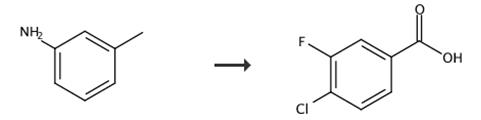
图4 4-氯-3-氟苯甲酸的合成路线[5]。
向反应釜中加入式(X)化合物和氯化亚砜,然后加入DMF,搅拌升温至70°C反应1.5h, 反应完成后降至室温,旋干后用氯仿溶解,降温至5 °C滴加30%氨水,滴加完成后稳定30min, 分层,取有机相加干燥剂,过滤,滤液旋干,然后加入三氯氧磷,搅拌升温至70°C反应1.5h, 然后降温至15°C旋干,加入二乙醚与水的混合液,降温至10°C并搅拌30min,分层取有机相,用饱和碳酸氢钠水溶液和饱和氯化钠水溶液洗涤,然后加入干燥剂,过滤,旋干,得到4-氯-3-氟苯甲酸。合成路线图如图4所示。
应用
4-氯-3-氟苯甲酸是重要的精细化工中间体,由于其分子结构中活性位点较多,可广泛应用于医药、农药、染料、生物工程、聚酯化合物等的合成[6-7]。我国从20世纪80年代开始研究开发 4-氯-3-氟苯甲酸,除农药领域有所应用外,医药等其他领域均处于起步阶段,且生产规模较小,产能低。随着精细化工产业的日益发展,4-氯-3-氟苯甲酸作为新型产品,应用范围不断扩大,需求量逐年增长,市场缺口越来越大。因此,开发并优化4-氯-3-氟苯甲酸的合成工艺,提高产能具有重要意义[8-9]。此外,在新型活性染料开发过程中,染料的提升力,耐水洗牢度一直是研究的重点和难点。4-氯-3-氟苯甲酸分子结构中含有强大的吸电子基团,为分子提供了良好的偶合活性,可以作为偶氮染料的一种偶合组分,在合成活性染料方面有全新的应用[10]。4-氯-3-氟苯甲酸还可用于合成具有三脚架构型的多吡啶类化合物以及高度支化聚合物等,在特殊功能材料等领域有良好的应用前景。具有三脚架构型的多吡啶类化合物通过氮的配位键、氢键、芳环与金属离子配位构建出结构新颖的配合物[11-12]。此外,该类化合物的侧链可自由翻转形成大小合适的空腔,能够与不同的客体结合,从而可以制备出具有特殊性能的功能材料[13]。
参考文献
[1] M. Altman, D.A. Candito, A.H. Christian, O. Di Pietro, M. Lu, P. Lui, U.F. Mansoor, K.M. Mennie, A.J. Musacchio, A. Palani, M.H. Reutershan, D.M. Shaw, S. St-Gallay, Cyclic cyanoenone derivatives as modulators of Keap1 and their preparation, Merck Sharp & Dohme Corp., USA; MSD R&D Innovation Centre Limited . 2022, p. 391pp.
[2] E.Y. Canales, W.K. Chang, L.P. Debien, P. Jansa, J.A. Loyer-Drew, L.P. Martinez, S. Perreault, G.B. Phillips, H.-J. Pyun, R.D. Saito, M.S. Sangi, A.J. Schrier, M.E. Shatskikh, J.G. Taylor, J.A. Treiberg, J.J. Van Veldhuizen, Preparation of macrocyclic bis-2,2'-azaindole derivatives as inhibitors of peptidylarginine deiminases, Gilead Sciences, Inc., USA . 2021, p. 1052pp.
[3] A.G. Cole, B.D. Dorsey, B.J. Dugan, Y. Fan, S.G. Kultgen, E.F. Mesaros, M.J. Sofia, Preparation of substituted (phthalazin-1-ylmethyl)ureas, N-(phthalazin-1-ylmethyl)amides, and analogues thereof for treating HBV and/or HDV infections, Arbutus Biopharma Corporation, Can. . 2021, p. 277pp.
[4] A.G. Cole, B.D. Dorsey, B.J. Dugan, Y. Fan, S.G. Kultgen, E.F. Mesaros, M.J. Sofia, Preparation of substituted isoquinolinylmethyl amides, analogues thereof for treating or preventing HBV and/or HDV infections, Arbutus Biopharma Corporation, Can. . 2021, p. 313pp.
[5] A.G. Cole, B.D. Dorsey, B.J. Dugan, Y. Fan, S.G. Kultgen, E.F. Mesaros, M.J. Sofia, Preparation of substituted tricyclic amides and analogs thereof, and methods using same, Arbutus Biopharma Corporation, Can. . 2021, p. 769pp.
[6] L.M. Delgado Oyarzo, G.A. Ureta Diaz, B. Pujala, D. Panpatil, S. Bernales, S. Chakravarty, Cycloalkylamine derivatives and related compounds as inhibitors of integrated stress response pathway and their preparation, Praxis Biotech LLC, USA . 2020, p. 395pp.
[7] K.A. Martin, C. Sidrauski, M.J. Dart, K.J. Murauski, J.T. Randolph, L. Shi, R.C. Smith, Y. Tong, X. Xu, H. Benelkebir, K.K. Chohan, S.J. Edeson, S. Schwenk, K.A. Starbuck, Preparation of heterocyclic compounds as modulators of the integrated stress pathway, Calico Life Sciences LLC, USA; AbbVie Inc.; Sygnature Discovery Limited . 2022, p. 708pp.
[8] K.A. Martin, C. Sidrauski, L. Shi, K.J. Murauski, X. Xu, Y. Tong, J.T. Randolph, M.J. Dart, H. Benelkebir, S. Edeson, K. Starbuck, Preparation of substituted cycloalkanecarboxamides as modulators of the integrated stress pathway, Calico Life Sciences LLC, USA; Abbvie Inc.; Sygnature Discovery Limited . 2020, p. 447pp.
[9] D. Meibom, Y. Cancho Grande, P. Wasnaire, S. Johannes, K. Beyer, T. Freudenberger, D. Brockschnieder, D. Zubov, D. Menshykau, B. Macdonald, Y. Xing, N. Elowe, G. Sanchez, Preparation of substituted hydantoinamides as ADAMTS7 antagonists, Bayer Aktiengesellschaft, Germany; Broad Institute . 2021, p. 556pp.; Chemical Indexing Equivalent to 175:47731 (WO).
[10] D. Meibom, Y. Cancho Grande, P. Wasnaire, S.A.L. Johannes, K. Beyer, T. Freudenberger, D. Brockschnieder, D. Zubov, D. Menshykau, T. Krainz, B. Macdonald, Y. Xing, N. Elowe, G. Sanchez, Preparation of substituted hydantoinamides as ADAMTS7 antagonists, Bayer Aktiengesellschaft, Germany; The Broad Institute, Inc. . 2021, p. 689pp.; Chemical Indexing Equivalent to 175:47728 (EP).
[11] N. Papaioannou, J.M. Travins, S.J. Fink, J.M. Ellard, A. Rae, Imidazopyridines as plasma kallikrein inhibitors and uses and preparation thereof, Charles River Discovery Research Services UK Limited, UK; BioDuro LLC; Shire Human Genetic Therapies, Inc. . 2021, p. 248 pp.
[12] S. Vendeville, P.J.-M.B. Raboisson, Synthesis of thiomorpholine dioxide compounds for treating hepatitis B viral infections, Aligos Therapeutics, Inc., USA . 2020, p. 179pp.
[13] C.-C. Wang, G.-X. Zhang, Z.-W. Zuo, R. Zeng, D.-D. Zhai, F. Liu, Z.-J. Shi, Visible-light-induced deep aerobic oxidation of alkyl aromatics, ChemRxiv (2021) 1-9.
