基本描述
BOC-D-亮氨酸的CAS号是16937-99-8,分子式是C11H21NO4,分子量是231.29。熔点是85-87°C(lit.),沸点是356.0±25.0°C(Predicted),密度是1.061±0.06g/cm3(Predicted)以及酸度系数(pKa)是4.02±0.21(Predicted)。BOC-D-亮氨酸一般易溶于二甲基亚砜,难溶于二氯甲烷和乙酸乙酯等。
天然氨基酸具有很好的生物营养价值,但是基本没有任何医药利用价值,相反,一些人工合成的非天然手性氨基酸在人体药物利用等方面拥有广阔的发展前景[1]。随着现代医学医药的不断发展,非天然手性氨基酸BOC-D-亮氨酸的临床应用范围越来越大。由于BOC-D-亮氨酸属于疏水性氨基酸,具有一个占分子空间大的线性链,所以它在多肽生物合成中能有效地控制多肽分子构象,增加多肽受酶催化降解的分子稳定性,保留原蛋白质中的有效利用价值,故而在生物、化学、医药方面广泛发展[2-3],可用作营养强化剂、动物饲用添加剂、作为合成医药中间体等,是合成抗艾滋病药物、肝炎病毒抑制剂等的合成前体[4]。

图1 BOC-D-亮氨酸的结构式。
合成
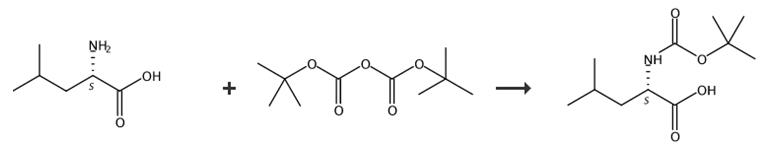
图2 BOC-D-亮氨酸的合成路线[5]。
向L-亮氨酸(8g,0.061mmol)在1,4-二恶烷(200ml)中的混合物中加入氢氧化钠水溶液(1N,8.5ml)和二叔丁基二碳酸酯(17.5g,80mmol),并将混合物搅拌过夜。蒸发溶剂后,用水(50毫升)稀释残留物,并用乙酸乙酯(2 x 50毫升)洗涤。将水相调节至pH=2-3,然后用乙酸乙酯(3x50ml)萃取。合并的有机层用盐水(2 x 50 mL)洗涤,用无水硫酸钠干燥并浓缩得到产物BOC-D-亮氨酸。白色固体,产率(6.75g,48%)。MS(EI):m/e=232.2[m+H]+。合成路线如图2所示。

图3 BOC-D-亮氨酸的合成路线[6]。
将N-(叔丁氧羰基)-L-亮氨酸(5.50g,23.54mmol)、甲苯(2.93ml)和MIBK(37.4ml)加入带有搅拌器的烧瓶中。在搅拌下将混合物加热至93℃。在3.5小时内将浑浊溶液冷却至环境温度并搅拌过夜。将浆料冷却至0°C并在此温度下搅拌85分钟。在玻璃过滤器上分离晶体,用MIBK(2x10 mL)洗涤,并在40°C下真空干燥得到白色固体BOC-D-亮氨酸。收率为5.61g(48.8%)。合成路线如图3所示。
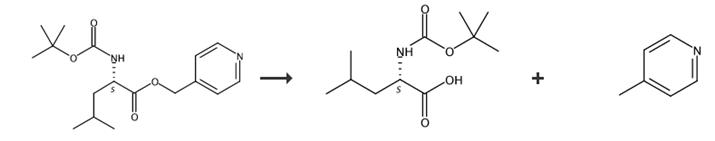
图4 BOC-D-亮氨酸的合成路线[7]。
将镁屑(288毫克,12毫摩尔)添加到微微醇N-Boc-L-丙氨酸-L-缬氨酸盐(0.76克,2毫摩尔)在甲醇(20毫升)中的溶液中。在室温下搅拌4小时后,过滤反应混合物。真空浓缩滤液,残留物用5%NaHCO3(10mL)和EtOAc(10mL),有机层用5%NaHCO3提取(2x10mL)。将水提取物用饱和硫酸钾酸化至pH 2-3,并用EtOAc(2x10ml)提取。有机层用盐水(2x10ml)洗涤,用Na2SO4干燥,并过滤。使用EtOAc PE通过硅胶柱层析纯化残余物BOC-D-亮氨酸。[α] D20-23.9(C1,AcOH)。合成路线如图4所示。
应用
BOC-D-亮氨酸是合成抗病毒药物阿扎那韦的关键侧链。抗癌药物 BB-2516、抗艾滋病药物阿扎那韦、抗炎药物 RO-31-9790、抗丙肝病毒药物特拉匹韦等药物的制备都需要借助BOC-D-亮氨酸进行合成[8-9]。BOC-D-亮氨酸常常替代其他氨基酸:如缬氨酸、亮氨酸等应用于多肽合成中,BOC-D-亮氨酸用作不对称反应的催化剂,在用作不对称氨化还原反应中化学酶催化剂的配体时能很好地提升其催化效率[10]。
随着工业技术和科学研究的发展,制备BOC-D-亮氨酸从最初的化学合成法到现在的生物催化法,实现了从高成本到低成本,高污染到低污染,高能耗到低能耗的转变BOC-D-亮氨酸作为很多药物合成的中间体,在生物领域、化工领域、医药领域等都具有十分重要的作用[11-13],因此对BOC-D-亮氨酸的合成路线的研究将一直作为热门项目,吸引一批又一批的科学家及研究人员不断探索、不断创新。
参考文献
[1] B. Bidi, A. Olgun, Biochemical medical diagnostic kit, Argeron Medikal Arastirma Sanayi ve Ticaret Anonim Sirketi, Turk. . 2022, p. 11pp.
[2] H. Feng, M. Dolejsi, N. Zhu, P.J. Griffin, G.S.W. Craig, W. Chen, S.J. Rowan, P.F. Nealey, Synthesis and Characterization of Block Copolymers for Nanolithography Based on Thiol-Ene "Click" Functionalized Polystyrene-Block-Polybutadiene, Adv. Funct. Mater. (2022) Ahead of Print.
[3] D. Guenther, C. Kalischer, O. Oeckler, A new modification of oxonium trimetaphosphimate monohydrate, Z. Anorg. Allg. Chem. (2022) Ahead of Print.
[4] F. Li, Z. Huang, S. Mo, S. Gu, S. Zhang, B. Yang, J. Wang, Z. Hu, Y. Zhang, Two undescribed pairs of isoprenyl hydroxybenzoic acid derivatives from coculture of Pestalotiopsis sp. and Penicillium bialowiezense: enantioseparation and their absolute configurations, New J. Chem. (2022) Ahead of Print.
[5] K. Lin, J. Lan, T. Zhu, Electrosynthesis of β-Acyloxy-γ-Selenyl Amines via Migratory Oxyselenation of N-Acyl Allylamines, Adv. Synth. Catal. (2022) Ahead of Print.
[6] F. Ma, S. Ma, Z. Yang, D. Ma, W. Hu, A kind of chiral n-boc/cbz-cis- (1 r, 2 s)-cyclohexanediamine method for preparing [Machine Translation], Shanghai Hanhong Technology Co., Ltd., Peop. Rep. China . 2022, p. 6pp.
[7] V.B. Mistry, H.B. Patel, P.P. Dedhiya, K.B. Bodiwala, S.R. Lodha, S.V. Joshi, G.G. Kalyankar, Design of experiment mediated development of stability indicating high performance thin layer chromatography method invoking failure mode effect analysis based risk assessment in estimation of edoxaban tosylate monohydrate, Indian J. Pharm. Educ. Res. 56(2) (2022) 553-563.
[8] P. Panwaria, M. Juanes, K.K. Mishra, R. Saragi, K. Borish, I. Usabiaga, A. Camiruaga, J.A. Fernandez, A. Lesarri, A. Das, Microhydration of Phenyl Formate: Gas-Phase Laser Spectroscopy, Microwave Spectroscopy, and Quantum Chemistry Calculations, ChemPhysChem (2022) Ahead of Print.
[9] J. Rao, Z. Wang, Y. Yue, Y. Shen, F. Lu, L. Lin, S. Ke, A kind of n-methyl piperazine hydrochloride preparation method of -d3- [Machine Translation], Anqing Roundcare Pharmaceutical Co., Ltd., Peop. Rep. China . 2022, p. 9pp.
[10] Q. Sheng, Y. Huang, Method and plant for the production of copper sulphate monohydrate [Machine Translation], Wujiang Weishida Copper Technology Co., Ltd., Peop. Rep. China . 2022, p. 9pp.
[11] H. Suzuki, K. Ichinohe, M. Araki, S. Muramatsu, T. Uehara, Y. Arano, Synthesis and evaluation of a para-carboxylated benzyl-DOTA for labeling peptides and polypeptides, Nucl. Med. Biol. 114-115 (2022) 18-28.
[12] J.A. Swift, M. Fleming, T. Watts, D. Hooks, Cooperative molecular motions in a nucleobase hydrate under thermal and mechanical stress, American Chemical Society, 2022, pp. MARM-54.
[13] S. Yang, S. Chen, C. Wang, S. Zhang, S. Li, X. Yuan, F. Peng, Y. He, Advances in research at synthesis process optimization and quality standard improvement of O-desmethylvenlafaxine succinate, Front. Chem. (Lausanne, Switz.) 10 (2022) 860292.
