背景及概述
MK-2206 2HCl是由美国 Merck 公司研究发现的个进入临床研究阶段的 Akt 小分子变构抑制剂。最初研究人员筛选发现,MK-2206不仅具有一定的 Akt 抑制活性,还对 Akt的不同亚型有一定选择性。Akt 在激活之前主要以“PH-in”的构象存在,PH 结构域与激酶催化区处于一种折叠的状态,两区域之间会产生特殊的变构位点(位于短肽 Link 上),而 MK-2206 2HCl能与此变构位点结合,锁定 Akt 的“PH-in”状态,限制 Akt 发生构象改变,进而抑制 Akt 激活,也阻止 Akt 调节的下游信号分子[包括结节性硬化症 2 蛋白(tuberous sclerosis complex 2,TSC2)、PRAS40 及核糖体 S6 蛋白]的磷酸化作用。由于Akt 的 3 种亚型在此变构位点存在一定差距,因此MK-2206 2HCl能在一定程度上实现 Akt 亚型间的选择性(Akt1、Akt2 和 Akt3 的 IC 50 分别为 8,12,65 nmol·L-1 )[1]。
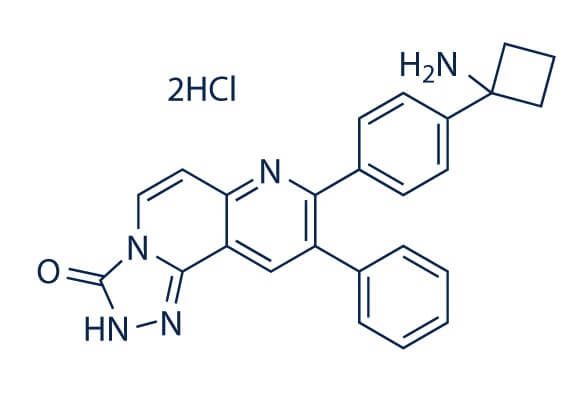
图1 MK-2206 2HCl结构式
临床前研究
临床前研究发现,MK-2206 2HCl在细胞水平对 Akt的 3 个亚型的抑制活性都达到了纳摩尔水平。与抑制 Ras 突变型细胞系(如 NCI-H358、NCI-H23、NCI-H1299 和 Calu-6)相比,MK-2206 2HCl更能有效抑制 Ras 野生型细胞系(如 A431、HCC827 和NCI-H292)。当与细胞毒素药剂如厄罗替尼和拉帕替尼联用,作用于肺部 NCI-H460 肿瘤细胞或卵巢A2780 肿瘤细胞,MK-2206 显示出协同效应。与细胞毒素药剂联用作用于 NCI-H292 移植瘤,MK-2206 也显示出非常有效的抗癌活性。
总结与展望
鉴于其较佳的临床前研究数据,MK-2206 2HCl的临床进展十分迅速。目前,针对 MK-2206 的多项Ⅰ期和Ⅱ期临床试验已经完成。在Ⅰ期临床试验中,MK-2206 表现出良好的安全性和耐受性;其针对局部晚期或转移性肿瘤的Ⅰ期临床试验也展现较好疗效;MK-2206 针对铂-耐药的复发性卵巢、输卵管或腹膜癌的Ⅱ期临床研究也已顺利完成。目前,针对 MK-2206 的临床Ⅲ期研究还没有报道。而对 Akt 小分子变构抑制剂的研究,主要集中在对 MK-2206 2HCl 类化合物进一步的结构优化,这也限制了该类变构抑制剂的迅速发展。
参考文献
[1]NCT01002248. Assessment of efficacy and safety of perifosine, bortezomib and dexamethasone in multiple myeloma patients [EB/OL]. 2014-02-14.
