基本信息
4-甲基-2-(1,1,1-三氟-2-二甲基-2-乙基)吡啶,英文名:4-Methyl-2-(1,1,1-trifluoro-2-Methylpropan-2-yl)pyridine,CAS号:1378865-93-0,分子量:203.204,密度:1.1±0.1 g/cm3,沸点:190.2±40.0 °C at 760 mmHg,分子式:C10H12F3N,闪点:68.8±27.3°C,蒸汽压:0.8±0.4 mmHg at 25°C,无色油状物,室温干燥密封保存。

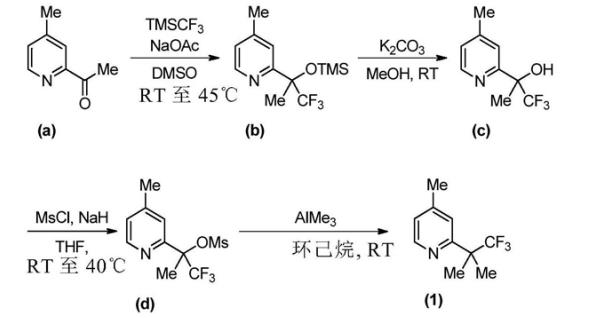
合成方法
S1、向溶于1L DMSO中的乙酸钠(96.0g,117mmol,1.0当量)中添加2-乙酰基-4-甲基吡啶(158g,117mmol,1.0当量)。再以另一0.5L DMSO稀释后,历时75分钟添加三甲基三氟甲基硅烷(375g,264mmol,2.2当量)。在添加期间将反应容器置于10℃的冷却浴中以保持介于20至25℃之间的内部温度。在室温下,搅拌所得黑色悬浮液,然后历时20分钟小心添加1.5L水中止反应。在加水期间,将反应容器置于-5℃的冷却浴中以保持介于10至25℃之间的内部温度。在室温下搅拌45分钟后,混合物以3L乙酸乙酯稀释及再搅拌15分钟。相分离,及水层以2L乙酸乙酯萃取。合并的有机相以3L饱和NaHCO3水溶液洗涤,在MgSO4上干燥,过滤及真空浓缩,从而产生346g呈棕色强烈气味的油的三氟甲基化合物(b)。
S2、在室温下,向溶于1.5L MeOH中的4-甲基-2-(2,2,2-三氟-1-甲基-1-三甲基硅烷氧基-乙基)吡啶(b)(346g,125mmol,1.0当量)的溶液中添加固体K2CO3(344g,249mmol,2.0当量)。在室温下搅拌所得米色悬浮液1小时,然后透过滤纸过滤。真空浓缩滤液,以产生固体、强烈气味的残质。将残质溶于1L乙酸乙酯中并以水(2×1L)洗涤。在MgSO4上干燥及过滤,真空浓缩后,得到油状物的252g(98%)醇(c)。
S3、向在0℃的NaH(60%溶于矿物油中,23.4g,585mmol,1.5当量)溶于1L THF中的悬浮液历时34分钟滴加1,1,1-三氟2-(4-甲基吡啶-2-基)丙-2-醇(c)(80g,390mmol,1.0当量)溶于200ml THF中的溶液。出现气体逸出,及反应混合物变为棕色。将反应温度升至40℃并搅拌45分钟,此时气体停止逸出。冷却至室温后,经30分钟滴加甲磺酰氯(45.6ml,585mmol,1.5当量)溶于50ml THF中的溶液。内部温度升至36℃,及反应混合物变为淡棕色悬浮液。将反应混合物升温至40℃下搅拌15分钟,冷却至室温搅拌过夜。在冰浴中小心添加750ml水中止反应。在室温下,搅拌所得棕色双相混合物30分钟,然后相分离。水层以750ml乙酸乙酯萃取,及合并的有机相以饱和NaHCO3水溶液洗涤。在MgSO4上干燥,过滤及真空浓缩,得到米色固体。将残质再次溶于300ml乙酸乙酯中,然后经过硅胶柱纯化。真空浓缩,产生米色固体,其在回流下再次溶于400ml庚烷及150ml乙酸乙酯中。在烧结漏斗上趁热过滤后,产物在0℃下结晶。过滤收集晶体,以8:3的冷庚烷/乙酸乙酯(2×80ml)洗涤及干燥(50℃,10毫巴)整夜,从而产生94.0g(85%)呈白色晶体的甲磺酸酯(d)。
S4、向在10℃下的溶于60ml环己烷中的甲磺酸1,1,1-三氟-2-(4-甲基吡啶-2-基)丙-2-酯(d)(5.68g,20.1mmol,1.0当量)的悬浮液历时15分钟滴加溶于己烷中的AlMe3(2.0M,15.0ml,30mmol,23.0当量)。反应升温至室温及在室温下搅拌3小时。混合物小心加入100ml 0℃水而中止反应及在室温下搅拌15分钟。在细胞植绒(Cellflock)塞中过滤及以乙酸乙酯洗脱后,相分离。水层以乙酸乙酯萃取,及合并的有机相以水及饱和NaCl水溶液洗涤。在Na2SO4上干燥后,过滤及真空浓缩,产生呈浅棕色的油,经硅胶层析(己烷/TBME=9:1)纯化,从而得到无色油4-甲基-2-(1,1,1-三氟-2-二甲基-2-乙基)吡啶1.15g化合物(1),收率28%。
参考文献
[1]诺华股份有限公司. 2-氨甲酰环氨基脲衍生物的合成:CN201610412757.0[P]. 2020-01-03.
