背景及概述[1][2]
稀土金属是稀有元素的一类。为元素周期表第六周期第Ⅲ类副族中的17种元素,即钪、钇、镧、铈、镨、钕、钷、钐、铕、钆、铽、镝、钬、铒、铥、镱、镥等。硫酸铥具有银白色光泽,化学性质很活泼,易溶于稀酸,能形成稳定的络合物以及微溶于水的草酸盐、氟化物、碳酸盐、磷酸盐和氢氧化物等。在冶金、电子、原子能及化学工业等方面稀土元素均有较多的应用。稀土元素及其化合物对环境的污染影响与对生物体的效应,目前尚在研究中。硫酸铥为铥的硫酸盐,化学式为Tm2(SO4)3·8H2O=770.16,浅绿色晶体。能溶于水,不溶于乙醇。将含有硫酸及氯化铥的混合溶液注入95%乙醇中,析出沉淀即得。
结构
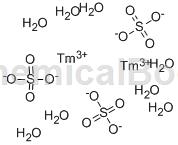
制备方法[1]
室温通过溶解相应的镧系元素氧化物(Tm2O3,Auer,99.99%)(75.6mg/80.1mg,0.20mmol)、2NH2SO4(Merck,p.a,96.0%)(10ml,0.020mol)。之后在室温下蒸发数周,可获得吧无色硫酸铥Tm2(SO4)3·8H2O的单晶。
主要参考资料
[1] 环境科学大辞典
[2] Syntheses,crystalstructuresandopticalspectroscopyofLn2(SO4)38H2O(Ln¼Ho,Tm)andPr2(SO4)34H2O
