肿瘤干细胞( Cancer Stem Cells, CSCS)
肿瘤干细胞假说认为肿瘤细胞中有部分细胞具有自我更新、增殖、多向分化潜能,它们与癌症转移、复发或肿瘤药物抗性的相关,这群细胞被定义为肿瘤干细胞[1,2]。
对于癌症干细胞研究人员来说,如果能从肿瘤细胞中分离、培养肿瘤干细胞,建立可靠的肿瘤模型,进一步揭示肿瘤干细胞的功能特性和肿瘤发生机制,从而靶向消除干细胞样癌细胞群。该方案将有望成为治疗恶性肿瘤的可靠策略之一。
基于文献阅读,小编今天和大家一起了解下如何从肿瘤细胞中分离培养肿瘤干细胞并建立肿瘤球模型。
建立培养法原理
常见三种分离CSCs的方法包括:建立培养法、MACS (磁性细胞分选) 和流式分选 (FACS) 。因篇幅有限,今天我们先看看便捷有效的建立培养法。
建立培养法乃基于肿瘤干细胞的生长特性,即在无血清、非贴壁的培养条件下,分化的肿瘤细胞将会死亡,而具有干性的肿瘤细胞会存活并增殖形成漂浮的细胞球[3],如下图。
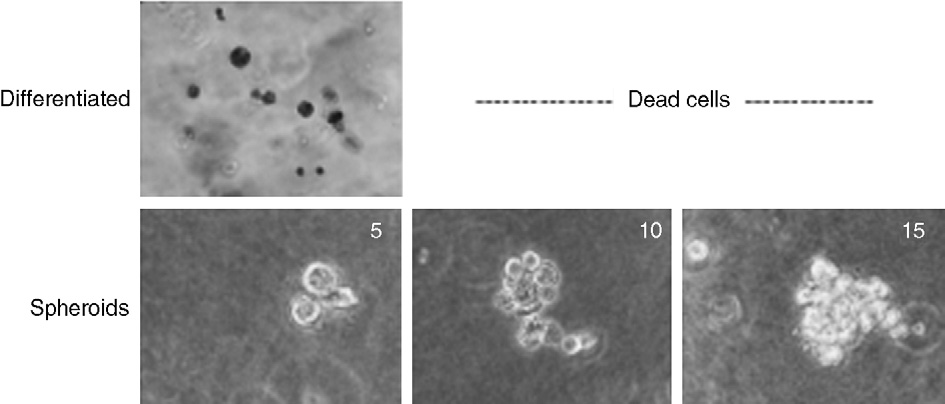
Fig. 1.Morphology of anchorage-independent growth performed in soft-agar up to 15 days cultures
from primary colon cancer cells and disaggregated colon cancer sphere cells (40X).图片来源于文献3
肿瘤球培养步骤
虽然肿瘤球的来源和类型不同,但在体外扩增培养的流程基本一致[4]。简单来说,将肿瘤组织经酶消化或机械分离成单细胞悬液后,接种在含无血清培养基的超低黏附细胞培养板或培养瓶中(注意不要贴壁),培养过程中可以适当补充生长因子,如EGF, FGF。在此条件下,肿瘤干细胞将缓慢增殖,约1-2个月形成非粘附肿瘤球。
下面我们以神经胶质瘤为例[5]。
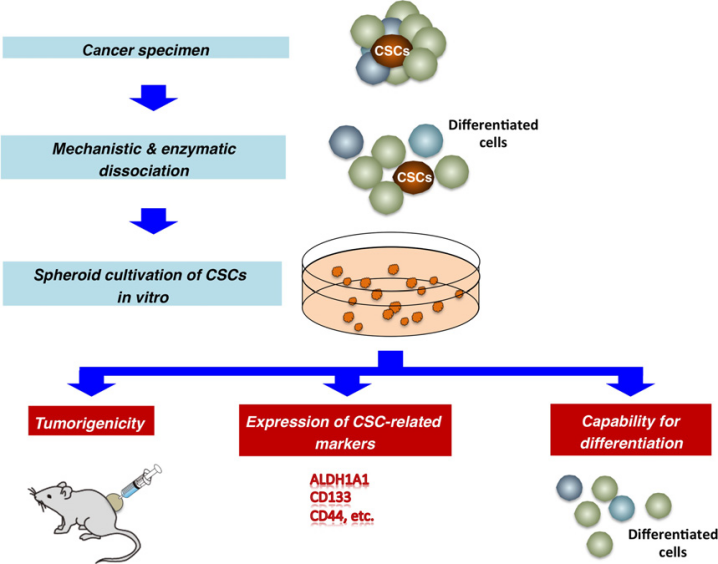
Fig. 2. General protocols for the establishment of tumor-derived spheroids. CSC, cancer stem cell.
图片来源于 © 2017 The Authors. Cancer Science published by John Wiley & Sons Australia, Ltd on behalf of Japanese Cancer Association.
1、将肿瘤组织样本在含有双抗的无菌PBS中洗涤、切碎并放入DMEM/F-12(Dulbecco 改良 Eagle 培养基/Ham 营养混合液 F12)无血清培养基(serum-free medium, SFM)中。
2、经酶或者机械法分离后通过40um的过滤器过滤,获得单细胞悬液。
3、再通过低渗裂解去除红细胞。
4、将细胞重悬于SFM中,活细胞计数。
5、以每毫升20,000个活细胞的密度铺板。(对于脑肿瘤干细胞球,可以使用两种条件:单独的SFM和补充有EGF,FGF2和硫酸肝素的SFM)。
6、每周更换培养基。用SFM或含有EGF 和 FGF2的SFM等体积培养基替换原培养基的一半。最快一周后出现肿瘤球。
7、球体至少生长3周且直径约100-200 um进行下游实验,如CSCs鉴定、体内成瘤实验或者诱导分化。
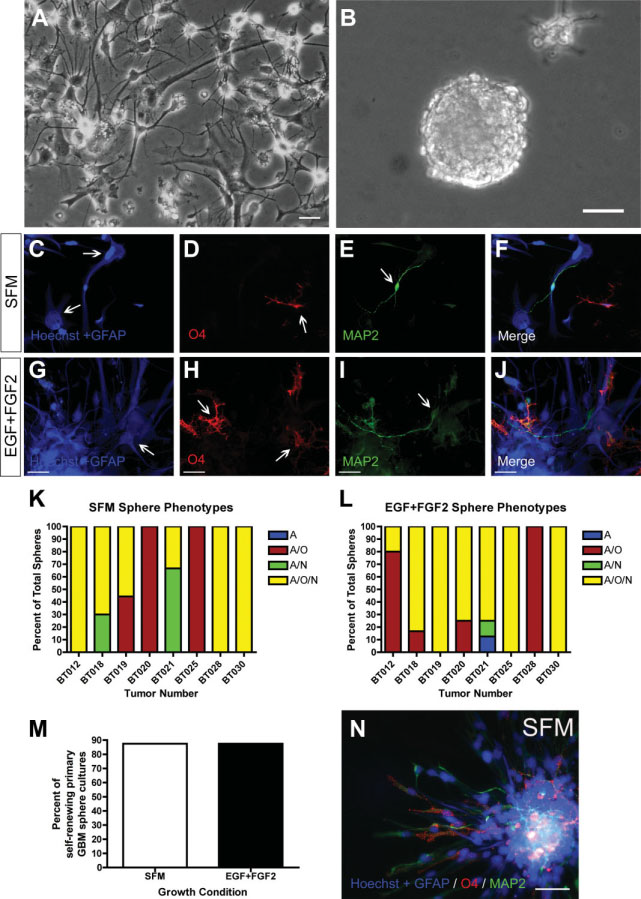
Figure 3. GBM brain tumor stem cells (BTSCs) proliferate into multipotent spheres and self-renew without exogenous mitogenic stimulation. (A, B): Phase-contrast photomicrographs demonstrate the typical appearance of GBM cells grown using the neurosphere culture system in SFM alone (without EGF þ FGF2); a monolayer of differentiated cells (A) and a floating GBM sphere (B).
图片来源于 Proliferation of Human Glioblastoma Stem Cells Occurs Independently of Exogenous Mitogens GBM BTSC Sphere and Human Temporal Lobe Cell Culture
Cultrex 3-D Spheroid Colorimetric Assay, 96-well
Cultrex 3D Spheroid Cell Invasion Assay
Cultrex 3-D Spheroid Fluorometric Assay, 96-well
Recombinant Human FGF-basic
Sterile 1x Dulbecco’s Phosphate Buffered Saline
Dulbecco 改良 Eagle 培养基/Ham 营养混合液 F12
青链霉素溶液,10KU青霉素和10mg链霉素/mL(双抗)
CSC的鉴定
CSCs表面表达一些特定的标志物,如CD44, CD133等,一般通过流式细胞术、免疫细胞化学、免疫荧光,WB等方法进行鉴定。另外,细胞内乙醛脱氢酶(ALDH)活性也是CSCs标志物之一。
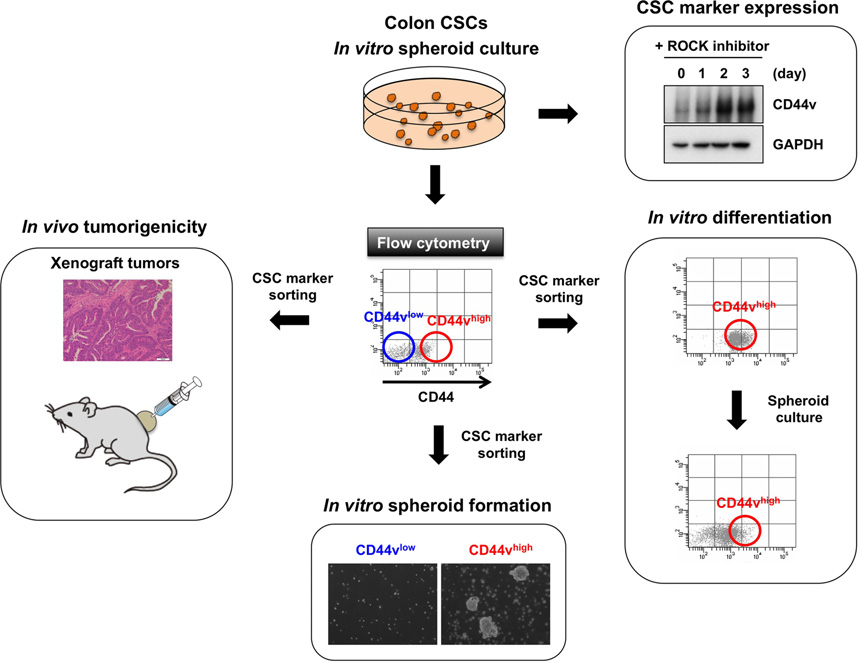
Figure 4. Evaluation of cancer stem cell (CSC)-associated phenotypes of colon spheroids derived from colorectal cancers. The CSC-associated phenotypes were validated based on CSC marker expression, flow cytometry, in vivo tumorigenicity, in vitro spheroid formation, and in vitro differentiation.
图片来源于 © 2017 The Authors. Cancer Science published by John Wiley & Sons Australia, Ltd on behalf of Japanese Cancer Association.
下表列出部分肿瘤干细胞标志物[2]。
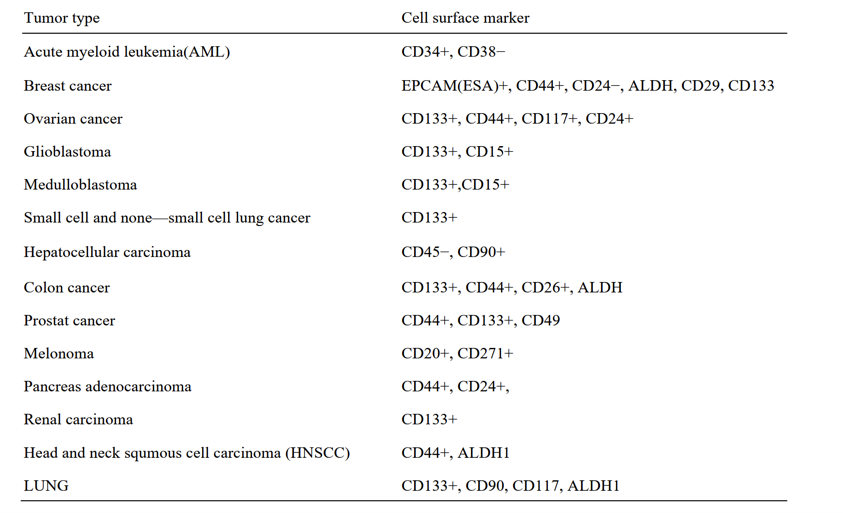
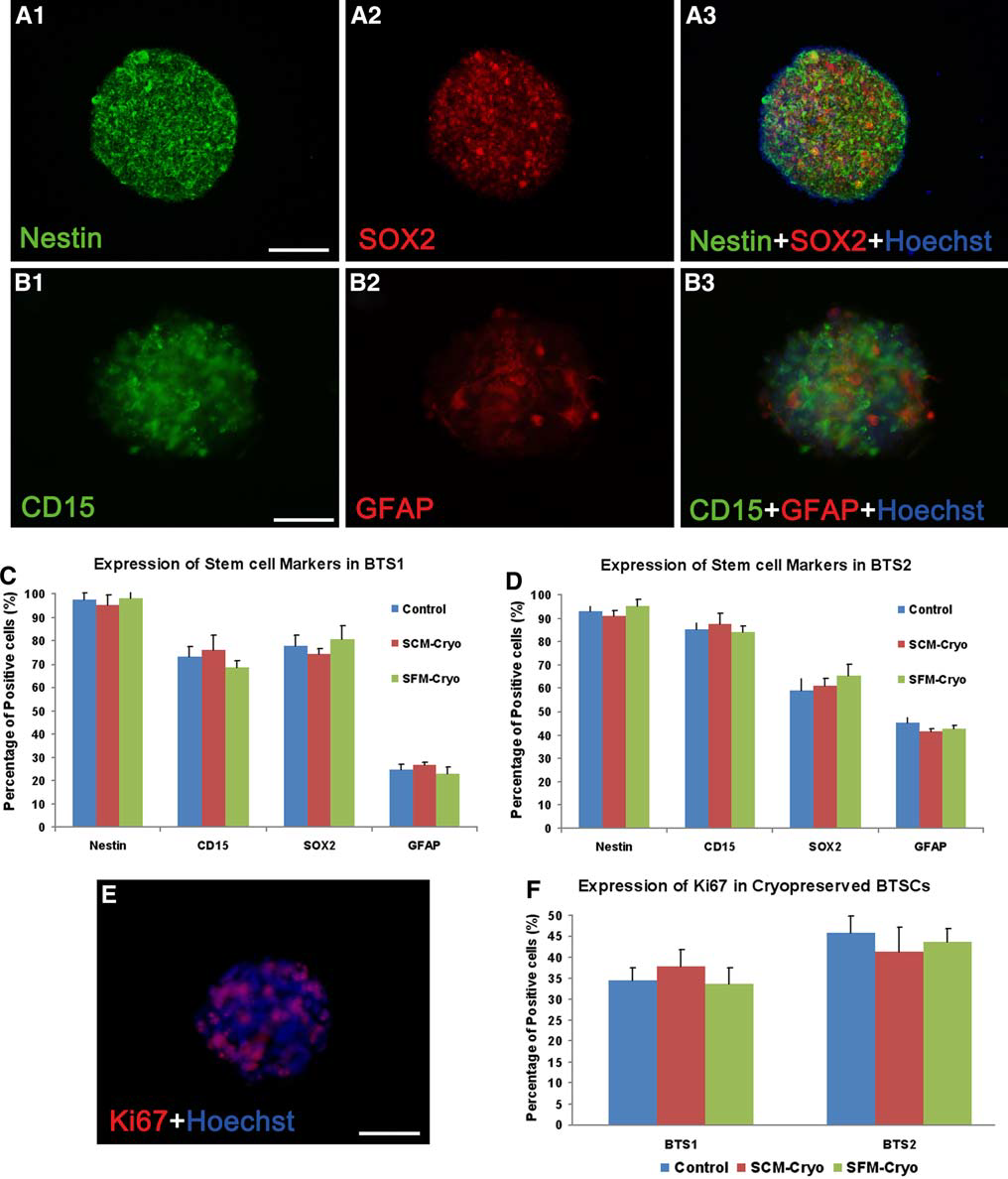
Figure 5. Expression of stem cell markers and proliferation marker in BTSCs before and after cryopreservation. Representative image of BTSCs(Brain tumor stem cells) cryopreserved in SFM and 10% DMSO. a and b stem cell markers nestin,SOX2, CD15, and GFAP expressed in BTSCs before and aftercryopreservation, 400X. 图片来参考文献6
Cultrex Basement Membrane Extract, Type 3, Pathclear
Human Magnetic Luminex Assay
Human CD44 Antibody MAB6127
Tumor Dissociation Kit, human
CD133 MicroBead Kit - Tumor Tissue,human
R&D提供Luminex 检测试剂盒,单孔可同时检测多达100种分析物,利用96孔板操作方便,实现高通量蛋白的精确定量。
肿瘤干细胞球的冻存与复苏
冻存和复苏操作基本同常规方法[6]。
冻存:将肿瘤球处理成单个细胞,然后将其重悬在含有10%二甲基亚砜(DMSO)的SFM培养基中梯度冻存(-80°C冰箱放置24小时,然后转至液氮储存6个月)。
复苏:37°C水浴1–2分钟,并用过量DMEM/F12洗去冻存液后置于SFM培养基中培养。
肿瘤球培养的局限性和难点
肿瘤球中丰富的CSCs为CSC特性评估和靶向药物提供了一个简易平台,但对于研究肿瘤微环境结构的内在特性却不是一个很好的模型,这时候就需要肿瘤类器官做深入研究。
肿瘤球培养的另一个局限性在于组织来源的球状体的长期培养具有挑战性,这可能是由于提取和维持活细胞的固有技术困难导致,而类器官可以相对稳定培养一年及以上。
细胞培养常见问题
1、3D培养与2D培养的区别与优势
回复:3D 培养通过模拟三维细胞网络、细胞与基质、细胞与细胞之间的相互作用,更贴近肿瘤组织相应的病理生理特征。
2、球体培养与类器官的差异
回复:球体培养与类器官的差异如下,
球体培养无需支架,通过贴壁细胞趋向于聚集的特性形成细胞球体,是用于 3D 细胞培养的最常见、最通用的无支架方法之一,常用的球体包括胚胎小体、乳腺球、肿瘤球体、肝细胞球和神经球,用于CSC研究。
类器官的构建依赖于有支架的 3D 培养,是高阶版的3D培养方法。类器官是体外展现真实器官的三维构造及生理功能的结构,虽然类器官通常较为小巧(直径 ≤ 3 mm),但它们是器官和组织的稳定模型系统,适合长期培养和操作,可用于疾病模型建立、药物筛选平台构建甚至是细胞移植(联系univ销售可免费申领3D类器官手册)。
3、细胞生长缓慢的可能原因及解决方案
回复:细胞生长缓慢有多种因素,常见可能原因包括如下,
1)生长培养基是否使用正确,需按照细胞说明书,使用预热的生长培养基。像干细胞需要添加不同比例的多种生长因子
2)生长培养基中血清质量差,可以使用其他批次血清做对照。
3)细胞传代次数过多,更换传代次数较少的细胞。
4)细胞生长超过汇合状态,哺乳动物细胞传代应在细胞处于对数期、未达到汇合状态时进行。
5)细胞被支原体污染。将细胞、培养基和试剂丢弃,新取一支冻存细胞,并且使用新的培养基和试剂。
4、常见细胞计数方法的优劣势对比?
回复:常见细胞计数方法包括计数板、流式细胞仪、细胞计数器计数。
1)计数板计数。细胞经台盼蓝染色后,取细胞重悬液于细胞计数板,然后在显微镜下观测并且手工计数。该法操作简便,无需特殊仪器,但过程费力且计数不准确。
2)荧光染料流式计数。该法较台盼蓝染色更准确与灵敏。其中碘化丙啶(Propidium Iodidi,PI)是应用最广泛的一种染料。流式细胞仪能够准确的计数,并且进行统计学分析,但是设备昂贵,需要有经验的实验人员进行专门操作,以及需要一定的设备维护等。
3)细胞计数器计数。库尔特原理被行业内作为细胞计数金标准,但常规的计数仪设备昂贵,操作不方便。基于以上缺陷,默克推出Scepter 3.0 手持式细胞计数器。Scepter Sensors 采用“计数金标准”库尔特原理,可以实现便捷、快速,准确地活细胞定量。
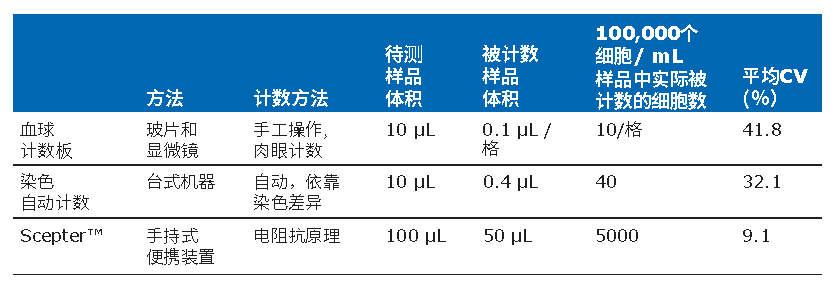
比较不同的技术方法
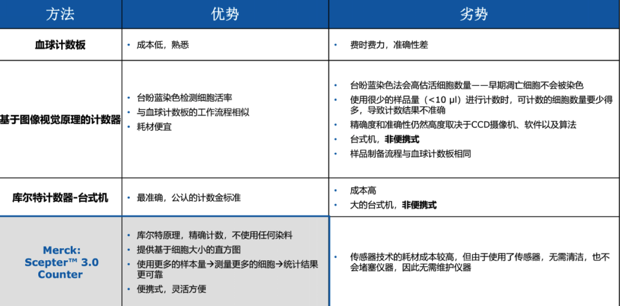
参考文献:
[1] Lapidot T, Sirard C, Vormoor J, Murdoch B, Hoang T, Caceres-Cortes J, Minden M, Paterson B, Caligiuri MA, Dick JE. A cell initiating human acute myeloid leukaemia after transplantation into SCID mice. Nature. 1994 Feb 17;367(6464):645-8. doi: 10.1038/367645a0. PMID: 7509044.
[1] Atena M , Reza A M , Mehran G . A Review on the Biology of Cancer Stem Cells[J]. Stem Cell Discovery, 2014, 04(4):83-89.
[2] Cammareri P, Lombardo Y, Francipane MG, Bonventre S, Todaro M, Stassi G. Isolation and culture of colon cancer stem cells. Methods Cell Biol. 2008;86:311-24. doi: 10.1016/S0091-679X(08)00014-9. PMID: 18442654.
[3] Ishiguro T , Ohata H , Sato A , et al. Tumor‐derived spheroids: Relevance to cancer stem cells and clinical applications[J]. Cancer Science, 2017, 108(3).
[4] Proliferation of Human Glioblastoma Stem Cells Occurs Independently of Exogenous Mitogens[J]. STEM CELLS, 2010, 27(8).
[5] Mao X G , Guo G , Wang P , et al. Maintenance of Critical Properties of Brain Tumor Stem-like Cells After Cryopreservation[J]. Cellular & Molecular Neurobiology, 2010, 30(5):775-786.
上海优宁维生物科技股份有限公司
试剂 | 耗材 | 仪器 | 软件 | 定制 | 实验服务 | 供应链

免费热线:4008-168-068
咨询邮箱:info@univ-bio.com
订购商城:www.univ-bio.com
微信公众平台:优宁维抗体专家,欢迎关注!
小优博士(小程序):5大课堂, 让你的科研不再难!:www.univ-bio.com