概述[1]
盐酸缬更昔洛韦(valganciclovirhydrochloride,)是瑞士罗氏公司研发的口服抗巨细胞病毒(CMV)感染药物,2001年5月经美国FDA批准上市。临床用于治疗获得性免疫缺陷综合症(AIDS)患者因感染CMV所致急性视网膜炎,2003年5月扩大了其适应证,用于预防和治疗器官移植者继发CMV感染。本品是更昔洛韦(ganciclovir)的前药,口服后在肠道和肝脏细胞中被酯酶迅速水解成更昔洛韦,从而发挥药效,其口服吸收的生物利用度为60%,且毒性大大降低。
药理作用[2]
更昔洛韦在体内可抑制疱疹病毒的复制,包括单纯疱疹病毒、水痘-带状疱疹病毒、EB病毒和巨细胞病毒等,尤以对缺乏胸苷激酶的耐药毒株及巨细胞病毒的作用显著;此外,本品对乙肝病毒、腺病毒及疱疹Ⅵ病毒亦有较强作用。在药理上,本品在CMV感染的细胞中被感染诱导产生的脱氧鸟嘌呤激酶转化成单磷酸盐,然后被鸟苷酸激酶及磷酸甘油激酶代谢成更昔洛韦三磷酸盐。其在病毒感染细胞内的浓度可以高于非感染细胞100倍。更昔洛韦主要通过两种方式抑制病毒复制:①其三磷酸盐(GTP)竞争性地抑制三磷酸脱氧鸟苷与DNA聚合酶结合,从而抑制病毒DNA聚合酶;②直接掺入病毒DNA,抑制DNA合成,阻止病毒DNA链的延长,并且此作用通过GTP在CMV感染细胞中的积累而得以放大。
临床应用[1]
盐酸缬更昔洛韦主要用于治疗免疫缺陷患者CMV感染如视网膜炎、肺炎、胃肠炎、肝脏和中枢神经系统感染。更昔洛韦的主要特点是对CMV病毒及乙肝病毒感染的疗效高于目前应用的一般药物。体外实验证明,更昔洛韦具有较强的抗巨细胞病毒、HSV-1、HSV-2、水痘-带状疱疹病毒、EB病毒活性,其中对巨细胞病毒、E-B病毒的抑制活性比阿昔洛韦强50倍,比膦甲酸(foscarnet)强15~19倍。据Sadeo报道,更昔洛韦也能有效的抑制异源造血干细胞移植过程中的人类疱疹病毒6(HHV-6)的感染。另据报道,DNA聚合酶发生突变的HBV变异株,均对ACV和磷甲酸钠(PFA)显出耐药,但对更昔洛韦仍敏感,说明还存在另一种与ACV完全不同的作用方式。
常用剂量[3]
CMV视网膜炎:诱导期,900mg,po,q12h,疗程3周。维持期,900mg,po,qd,直至免疫重建(连续3~6个月CD4>150/μL,眼科检查证实病变稳定)。
胃肠道CMV病:900mg,po,q12h,疗程3~6周(病情严重或复发时考虑维持治疗)。
接受肾脏、心脏和肾脏—胰腺联合器官移植的CMV感染高危患者的预防:900mg,po,qd,自移植10天内开始,直至移植后100天。
副作用[3]
常见可逆性粒细胞减少(对G-CSF反应好)、血小板减少、腹泻、恶心。偶见贫血、发热、皮疹、头痛、头晕。罕见肝毒性、抽搐。
其他要点[3]
是更昔洛韦的前体药物,口服后迅速转化成更昔洛韦,需与食物同服。用药期间需监测血象;外周血中性粒细胞计数<500/μL停药或加用G-CSF;外周血血小板计数<25000/μL或血红蛋白<80g/L考虑停药;有中枢神经系统副反应者避免驾驶汽车和操作机械。
制备[2]
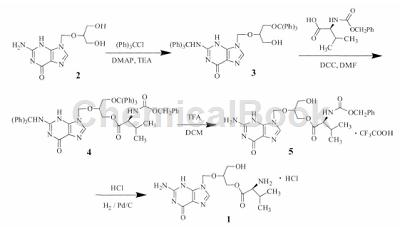
1)N,O-二(三苯甲基)更昔洛韦
2(20.5g,80mmol)、三乙胺(43.3g,428mmol)和4-二甲胺基吡啶(DMAP,47mg,0.4mmol)加入DMF(190ml)中,再滴加三苯基氯甲烷(59.5g,210mmol)的DMF溶液(190ml),滴毕升温至50℃,搅拌过夜。冰浴冷至10℃,搅拌2h,抽滤,滤饼用DMF(40ml)洗涤。滤液加入活性炭(2g),搅拌2h,抽滤。滤液中缓慢滴加去离子水(220ml),析出固体后再滴加去离子水(200ml),搅拌过夜,抽滤,水(50ml×3)洗,95%乙醇(50ml)洗,烘干得白色固体3(36.2g,60.9%),纯度98.1%[HPLC归一化法:色谱柱AgilentEclipseXDB-C18柱(4.6mm×150mm,5m);流动相A:水,B:乙腈,梯度洗脱(0→5min:B5%;5→30min:B5%→90%);检测波长254nm;流速1.0ml/min;柱温30℃;进样量10l](文献:收率63.2%,纯度90%),mp250~252℃。
2)N-苄氧羰基-L-缬氨酸2-[(2-三苯甲基氨基-1,6-二氢-6-氧代嘌呤-9-基)甲氧基]-3-(三苯甲基)氧基-1-丙酯(4)
N-苄氧羰基-L-缬氨酸(30.1g,120mmol)溶于二氯甲烷(60ml),加入DCC(12.4g,60mmol),室温搅拌20h。减压抽滤,二氯甲烷(30ml)洗涤,滤液减压浓缩,得到N-苄氧羰基-L-缬氨酸酐,加DMF(60ml)溶解,加入DMAP(1.0g,8.2mmol)后,滴加3(30.0g,40.5mmol)的DMF溶液(150ml),室温搅拌24h。倒入去离子水(600ml)中,用乙酸乙酯(800ml)萃取,有机相用饱和碳酸氢钠溶液(100ml)和水(100ml×2)洗涤,干燥浓缩得黏稠液体,经乙酸乙酯∶石油醚(2∶1,150ml)结晶,烘干得白色固体4(32.2g,81.5%),纯度98.8%[HPLC归一化法:流动相A:水,B:乙腈,洗脱梯度(0→20min:B60%→90%;20→25min:B90%);其他与3相同](文献:收率98.6%,纯度93.5%),mp180~182℃。ESI-MS(m/z):974[M+H]+;
3)N-苄氧羰基-L-缬氨酸2-[(2-氨基-1,6-二氢-6-氧代嘌呤-9-基)甲氧基]-3-羟基丙酯三氟乙酸盐(5)
4(30.0g,30.8mmol)溶于二氯甲烷(75ml),冰浴降至15℃以下,滴加三氟乙酸(120ml)和二氯甲烷(50ml)的混合液,室温搅拌16h。冰浴下倒入异丙醚(1.2L)中,搅拌2h,抽滤得白色固体5(16.4g,88.2%),纯度95.3%[HPLC归一化法:流动相A:水,B:甲醇,梯度洗脱(0→15min:B20%→80%,15→20min:B80%→90%,20→30min:B90%);
4)盐酸缬更昔洛韦
5(14.0g,23.2mmol)溶于甲醇(140ml),滴入浓盐酸(3.0ml),加入10%钯炭(1.0g),室温通入氢气,常压反应6h,TLC[展开剂:甲醇∶二氯甲烷(1∶5)]显示反应完毕,抽滤,浓缩滤液,加入去离子水(10ml)和异丙醇(80ml),升温回流0.5h,冷却结晶,抽滤,60℃真空烘干得白色固体1(7.1g,78.0%)。mp170~172℃(文献:收率90.2%,mp170~172℃)。纯度98.8%[HPLC归一化法:流动相A:0.1mol/L磷酸二氢铵溶液,B:甲醇,梯度条件(0→5min:B8%;5→15min:B8%→20%;15→30min:B20%→70%);其他与3相同],其中2含量1.0%,非对映异构体比例1.11,符合美国药典(USP35)要求(2含量低于1.5%,非对映异构体比例0.8~1.2,总纯度不低于97%)。ESI-MS(m/z):355[M+H]+;1HNMR(400MHz,CD3OD):0.96~1.01(m,6H),2.06~2.12(m,1H),3.59~3.69(m,2H),3.70~3.80(m,1H),3.98~4.08(m,1H),4.15~4.20(m,1H),4.36(d,J=10.8Hz,1H),5.61(s,2H),7.93(d,J=13.2Hz,1H)。13CNMR(100MHz,CD3OD):16.6,16.9,29.5,57.9,60.5,65.0,71.5,77.0,115.6,138.4,151.9,154.4,157.7,168.6。
主要参考资料
[1] 抗巨细胞病毒药物-更昔洛韦
[2] 盐酸缬更昔洛韦的合成
[3] 协和抗感染手册
