背景及概述[1]
氨基酸作为熟知的广泛的中性物质,由于具有氨基与羧基,使得氨基酸具有两性的性质,能够与其他物质形成分子间的相互作用。天冬酰胺具有一个十分重要的生物学意义,因为它是20个氨基酸的基本组成部分之一,存在于生物体中的许多蛋白质。

制备方法[2]
(1)将25公斤顺酐废渣加入到200升的自来水中,加热至85℃使废渣溶解,过滤除去不溶物,加入0.5公斤硫脲,用盐酸调节体系pH至3,加热回流2.5小时,冷却析晶,过滤得17.6公斤固体。
(2)将上述所得17.6公斤固体用180公斤自来水加热至90℃使其溶解,加2公斤活性碳加热回流1小时脱色,趁热过滤除杂,用氨水将滤液pH调至10,向滤液中加入44克大肠杆菌,反应5小时后用10wt%盐酸溶液调pH至6,冷却析晶,过滤得15.7公斤固体。
(3)将上述所得15.7公斤固体用157公斤乙醇在20℃下浸泡5小时,过滤得5.8公斤晶体,将所得晶体在80℃下烘8小时,得4.9公斤产品,即为天冬酰胺,HPLC含量为97.4%。
浓度检测方法[1]
一种检测溶液中天冬酰胺浓度的方法,包括以下步骤:
步骤一、制备所述工作电极并搭建三电极体系,配制浓度为0~1.5×10-4mol/L的6份天冬酰胺的标准溶液;
其中,所述步骤一中天冬酰胺的标准溶液配置方法为:向Tris-HCl缓冲溶液中加入浓度为0.01mol/L的天冬酰胺标准溶液,分别制备天冬酰胺浓度为0mol/L、3×10-5mol/L、6×10-5mol/L、9×10-5mol/L、1.2×10-4mol/L、1.5×10-4mol/L的6个标准溶液,并且每一份溶液中都含有1×10-4mol/L色氨酸;其中所述Tris-HCl缓冲溶液的pH为7.0,其浓度为0.01mol/L;
步骤二、采用所述三电极体系,利用差分脉冲伏安法对步骤一中配制的每份标准溶液进行检测,得到每份标准溶液的差分脉冲伏安曲线,在此过程中分别记录每份标准溶液的差分脉冲伏安曲线中电位值;
其中,所述步骤二具体包括以下步骤:
步骤2.1、将所述三电极体系分别置入所述六个标准溶液中,在室温下搅拌3min,静止3min;
步骤2.2、扫描差分脉冲图谱,设置扫描初始电位为-0.2V,终止电位为1.0V,电位增量为0.004V,样品宽度0.0167s,振幅为0.05V,脉冲宽度0.05V,灵敏度10-5A/V,等待时间为2s;
步骤2.3、分别测量并记录所述六个标准溶液的电流强度的峰值,建立所述六个标准溶液的差分脉冲伏安曲线,图1所示六个标准溶液的差分脉冲伏安曲线;
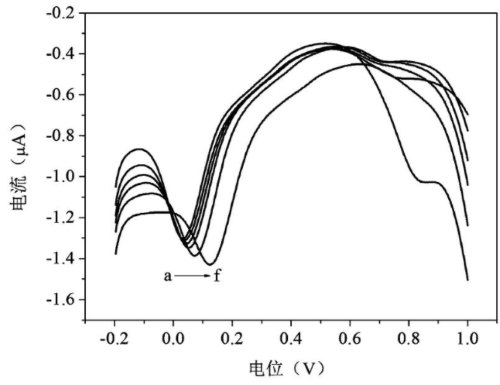
步骤三、以步骤二中得到的溶液b、c、d、e、f五个标准溶液的差分脉冲伏安曲线对应的电位值与溶液a的标准溶液的电位值的差值作为纵坐标,以溶液b、c、d、e、f中天冬酰胺的浓度为横坐标绘制标准曲线并计算线性方程;例如,以溶液b的差分脉冲伏安曲线对应的电位值与溶液a的标准溶液的电位值的差值为纵坐标,以溶液b中天冬酰胺的浓度为横坐标,可以确定标准曲线上的一个点,通过上述方法,将溶液b换成溶液c、d、e、f,通过溶液c、d、e、f确定标准曲线上的另外四个点,绘制如图2所示的标准曲线;
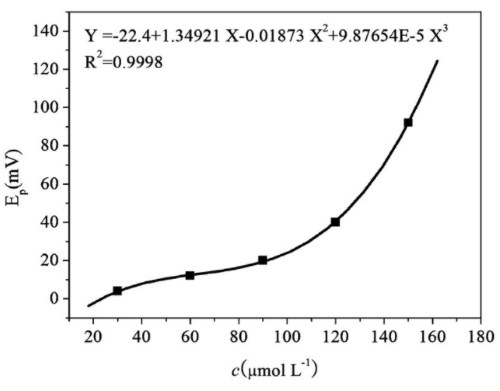
由图2中标准曲线得到线性方程:Y=-22.4+1.34921X-0.018X2+9.87654×10-5X3,式中Y为电流值(E-E0),E为每份标准溶液的差分脉冲伏安曲线对应的电位值;E0为天冬酰胺浓度为0mol/L时的标准溶液的电位值,单位为mV;X为标准溶液中天冬酰胺浓度,单位为μmol/L,相关系数R2为0.9998。工作电极对天冬酰胺的检测限为3.0×10-5mol/L;
步骤四、采用所述三电极体系,利用差分脉冲伏安法对含有未知浓度天冬酰胺的待测溶液进行检测,得到待测溶液的差分脉冲伏安曲线,计算待检测液中天冬酰胺的浓度:将待测溶液的差分脉冲伏安曲线对应的电位值与天冬酰胺浓度为0mol/L的标准溶液的电位值的差值作为Y值代入步骤三中得到的线性方程中,计算X值得到待测溶液中天冬酰胺的浓度。
参考文献
[1] [中国发明,中国发明授权] CN201610619894.1 检测溶液中天冬酰胺浓度的方法
[2] [中国发明,中国发明授权] CN201310488869.0 顺酐废渣用于制备天冬氨酸的用途和利用顺酐废渣制备天冬氨酸的方法
