背景及概述[1][2]
利那洛肽( linaclotide) 是由美国 Ironwood 公司研发的一种鸟苷酸环化酶 C(GC-C) 激动剂,于2012 年 8 月 30 日获美国 FDA 批准上市,商品名为 Linzess。该药为胶囊剂,用于治疗便秘肠易激综合征( IBS-C) 和慢性特发性便秘(CIC),它是首个具有此种作用机制的治疗便秘的药物。
利那洛肽是一个 14-氨基酸肽,序列为 L-cysteinyl-L-cysteinyl-L-glutamyl-L-tyrosyl-L-cysteinyl-Lcysteinyl-L-asparaginyl-L-prolyl-L-alanyl-L-cysteinylL-threonyl-L-glycyl-L-cysteinyl-L-tyrosine,cyclic (1-6),(2- 10),(5- 13) -tris( disulfide);为白色至灰白色无定形粉末;微溶于水和氯化钠水溶液( 0. 9% ) 。利那洛肽口服进入人体后通过与肠道中的鸟苷酸环化酶 C 型受体(GC-C)结合,使细胞内和细胞外环鸟苷酸(cGMP)浓度升高,刺激肠液分泌,加快胃肠道移行,从而增加排便频率,由于其独一无二的作用机制,很有希望成为一种不但可以治疗便秘,还可以治疗腹胀、腹痛和其它临床症状的治疗药物.。
规格[3]
胶囊:145 μg和290 μg。
用法用量[3]
1)IBS-C:290 μg口服每天1次;2)CIC:145 μg 口服每天1次;3)空胃服用首次餐至少30分前。
应用[3]
适用于在成年中为治疗:1)有便秘肠易激综合征(IBS-C) ;2)慢性特发性便秘(CIC)。
临床研究[1]
在临床进行的随机、双盲试验中,将 IBS-C 患者随机分为治疗组(给予利那洛肽 290 μg/d)和安慰剂组,治疗至少 12 周,结果显示,与安慰剂组相比,利那洛肽在患者腹痛和增加完全自发排便次数(CSBMs) 方面更有效。利那洛肽用于慢性特发性便秘患者的安全性和有效性,在进一步开展的两项双盲、多中心临床试验中得到了证实,在这两项研究中,患者被随机分为安慰剂组、利那洛肽145 μg/d组或利那洛肽 290 μg/d组。
治疗 12 周后,剂量为 145 μg/d利那洛肽治疗组的患者完全自发排便次数明显高于安慰剂组。而 290 μg/d治疗组的临床效果并没有太大的提高,故对于慢性特发性便秘( CIC) 的治疗 FDA 只批准了145 μg/d剂量。该药的推荐剂量为 290 μg/d (治疗 IBS-C) 和 145 μg/d (治疗CIC),于当天首餐前至少 30 min 服用。利那洛肽的不良反应包括腹泻、 腹痛和呕吐。值得注意的是,16 岁及以下的患者。
药理作用 [1]
利那洛肽是一种鸟苷酸环化酶 C 激动剂,它与肠道 GC-C 结合后,导致细胞内和细胞外环鸟苷酸( cGMP) 浓度升高。细胞内 cGMP 升高可以刺激肠液分泌,加快胃肠道移行,从而增加排便频率;细胞外 cGMP 浓度升高会降低痛觉神经的灵敏度、降低肠道疼痛。
药代动力学[3]
吸收:口服给药后LINZESS吸收少生物利用度低。口服剂量145 μg或290 μg给药后利那洛肽及其活性代谢物的浓度血浆中低于定量低限。因此,不能计算标准药代动力学参数例如曲线下面积(AUC),最高浓度(Cmax),和半衰期(t½)。
分布:鉴于利那洛肽治疗的口服剂量的血药浓度,是无法衡量的,预计利那洛肽分布至组织很少。
代谢:利那洛肽在胃肠道内通过丢失末端酪氨酸部分被代谢为其主要,活性代谢物。利那洛肽及其代谢物在小肠腔内被蛋白解降解为较小肽和天然存在氨基酸。
消除:进食和空腹受试者每天给予290 μg的LINZESS共7天后在粪样品中回收活性肽平均约5% (空腹)和约3% (进食)和实际上所有为活性代谢物。
不良反应[3]
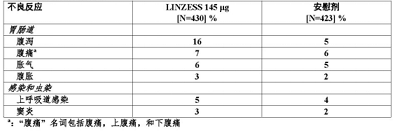
注意事项[3]
1. 儿童风险在患儿直至6岁LINZESS禁忌。在非临床研究中,在幼年小鼠中(1至3周龄小鼠;约等于人患儿小于2岁)给予1或2次每天口服剂量利那洛肽后死亡发生在24小时内。在6至17岁患者中避免使用LINZESS.利那洛肽不致死亡在较年长幼小鼠中(约等于人年龄12至17岁)。虽然在较年长幼小鼠中没有死亡,给予年青幼小鼠死亡和在青少年患者中缺乏临床安全性和疗效数据,在6至17岁患者中避免使用LINZESS。
2. 腹泻:在合并IBS-C和CIC双盲安慰剂对照试验中腹泻是LINZESS-治疗患者最常见不良反应。LINZESS-治疗患者报道的严重腹泻为2%。I BS-C和CIC人群间腹泻的发生率相似。
药物相互作用[3]
尚未进行药物-药物相互作用研究。给予推荐临床剂量后血浆中不能检测到利那洛肽及其活性代谢物;因此,预计无全身药物-药物相互作用或通过血浆蛋白结合利那洛肽或其代谢物介导的药物相互作用。根据体外研究结果利那洛肽与细胞色素P450酶系统不相互作用。此外,利那洛肽不是外流转运蛋白P糖蛋白(P-gp)的底物也不是其抑制剂。
制备[4][5][6]
方法1:一种制备利那洛肽的方法,包括以下步骤:
1)Fmoc-Tyr(tBu)-OH与载体树脂反应,得到Fmoc-Tyr(tBu)-树脂;
2)Fmoc-Tyr(tBu)-树脂与其他带有Fmoc保护基团的氨基酸逐一用活化剂偶联,得到利那洛肽线性肽树脂;
3)利那洛肽树脂经脱保护、裂解试剂裂解、得到利那洛肽线性肽;
4)利那洛肽线性肽中的三个二硫键经氨水/DMSO体系环化后,得到利那洛肽粗肽;
5)利那洛肽粗肽在碱性缓冲溶液中纯化后,冻干即得到利那洛肽纯品。
方法2:一种合成利那洛肽的方法,包括以下步骤:
步骤1、合成在SEQ ID NO:1所示氨基酸序列Thr侧链上、Cys侧链上、Asn侧链上、Tyr侧链上、Glu侧链上偶联有保护基以及在C端偶联有树脂载体的利那洛肽树脂;
步骤2、利那洛肽树脂酸解脱除所有保护基和树脂载体得到利那洛肽线性粗肽,然 后采用半胱氨酸盐酸盐/DMSO缓冲溶液对利那洛肽线性粗肽进行环化,按照其N端到C端的 氨基酸顺序,形成第1位Cys和第6位Cys的二硫键、第2位Cys和第10位Cys的二硫键以及第5 位Cys和第13位Cys的二硫键得到利那洛肽粗品,粗品纯化转醋酸盐后即得利那洛肽成品。
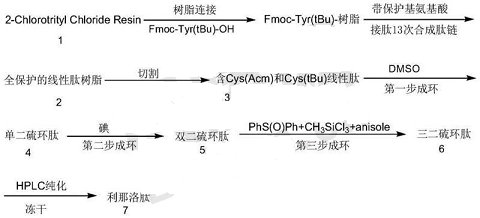
方法3:一种利那洛肽的固相合成方法,该方法包括如下步骤:
1)利那洛肽树脂的制备:Fmoc-Tyr(tBu)-OH和载体树脂反应,获得Fmoc-Tyr(tBu)- 树脂;以Fmoc-Tyr(tBu)-树脂为固相载体,采用逐一偶联的方式从C端到N端依次偶联 13个具有Fmoc保护基团的氨基酸,获得利那洛肽线性肽树脂,其中,形成二硫键的三 组Cys分别连接Trt、Acm或tBu保护基,同组的Cys连接相同保护基,不同组的Cys 连接不同的保护基;
2)将步骤(1)得到的利那洛肽线性肽树脂进行切割,脱去除Cys(Acm)和Cys(tBu) 外的所有氨基酸的侧链保护基,得到了含有Cys(Acm)和Cys(tBu)的保护基线性肽;
3)氧化步骤(2)得到的线性肽形成对二硫键,得到单二硫环肽;
4)脱除步骤(3)得到的单二硫环肽中Cys(Acm)中Acm保护基,同时形成第二对二硫键,得到双二硫环肽;
5)脱除步骤(4)得到的双二硫环肽中Cys(tBu)中的tBu保护基,同时形成第三对二硫键,得到三二硫环肽;
6)步骤(5)得到的三二硫环肽经HPLC制备纯化,冻干得到利那洛肽。
参考资料
[1] 卫高菲. 利那洛肽[J]. 中国药物化学杂志, 2013 (1): 78-78.
[2] 葛巍巍, 陈静, 张也, 等. 半选择性氧化形成三对二硫键合成利那洛肽[J]. 有机化学, 2017, 37(9): 2409-2415.
[3] 利那洛肽说明书
[4] CN201610644791.0 一种制备利那洛肽的方法
[5] CN201510314459.3 一种合成利那洛肽的方法
[6] CN201510391880.4 一种利那洛肽的固相合成方法
