多肽是一种由两个或多个氨基酸通过肽键(酰胺键)连接而形成的化合物。多肽在调节机体各系统、器官、组织和细胞的功能活动以及在生命活动中发挥重要作用,并且常被应用于功能分析、抗体研究、药物研发等领域。而通过对多肽进行修饰进而改变多肽的理化性质也是多肽研究中一种常用的手段。多肽修饰种类繁多,从修饰位点不同则可分为N端修饰、C端修饰、侧链修饰、氨基酸修饰、骨架修饰等(图1)。作为一种改变肽链主链结构或侧链基团的重要手段,多肽修饰可有效改变肽类化合物的理化性质、增加水溶性、改变其生物分布状况、延长体内作用时间、降低毒副作用、消除免疫原性等。今天我们来介绍几种最主要的多肽修饰及特点。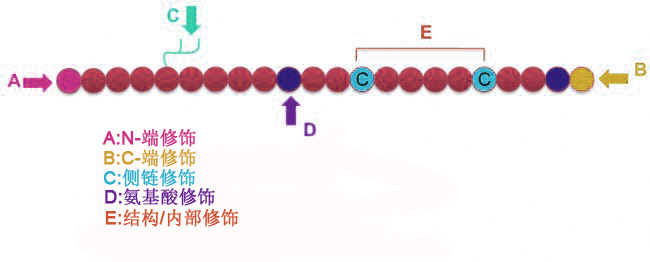 1、环化
1、环化
在自然界中,许多具有生物活性的多肽都是环状多肽,因此环肽在现代生物医学中有主多应用。环肽相较于线性肽,具有更好的刚性,对消化系统具有极强的抵抗力,因此可以在消化道中存货,并且对靶受体表现出更强的亲和力。环状多肽通常都是通过环化来实现的,根据环化方式可以分为侧链-侧链式、终端-侧链式、终端-终端式(头尾相连式)。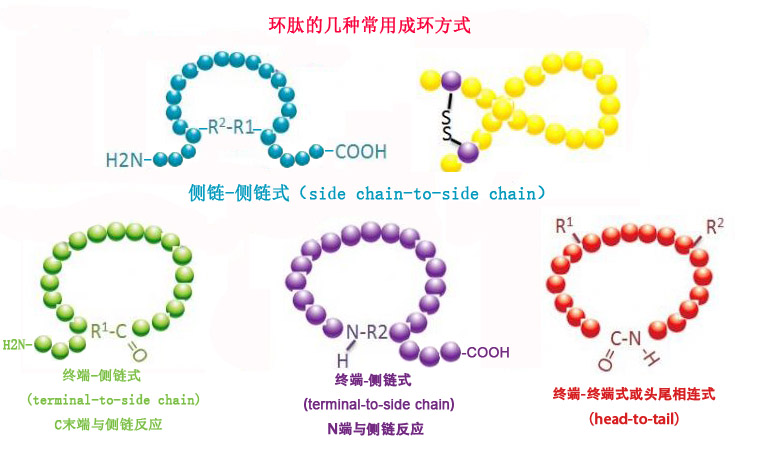 (1)侧链-侧链式(side chain-to-side chain)
(1)侧链-侧链式(side chain-to-side chain)
通过半胱氨酸残基间的二硫桥接是一种最常见的多肽成环方式,而这种方式就属于侧链-侧链式环化,引入这种环化的方法是通过一对半胱氨酸残基脱保护然后氧化构成二硫键。通过选择性地移除巯基保护基可以实现多环的合成。环化既可以在解离后的溶剂里完成,也可以在解离前的树脂上完成。由于树脂上的多肽不易形成可环化的构象,因此在树脂上环化可能要比在溶剂中环化低效。第二种侧链-侧链式环化类型是在门冬氨酸或谷氨酸残基与基础氨基酸之间形成酰胺结构,它要求多肽无论是在树脂上还是解离后,侧链保护基都必须能够选择性移除。第三种侧链-侧链式环化是通过酪氨酸或对羟基苯甘氨酸形成联苯醚,但是制备这些化合物需要独特的反应条件,因此不常用于常规多肽的合成。
(2)终端-侧链式(terminal-to-side chain)
终端-侧链式环化通常涉及C末端与赖氨酸或鸟氨酸侧链的氨基,或者N末端与门冬氨酸或谷氨酸侧链形成酰胺键而成环。还有一些多肽环化是通过末端C与丝氨酸或苏氨酸侧链形成醚键而构成。
(3)终端-终端式或头尾相连式(head-to-tail)
终端-终端式或头尾相连式是通过多肽N端氨基和C端羧基通过形成酰胺化而形成,链状多肽可以在溶剂中环化或者固定在树脂上通过侧链环化。在溶剂中环化应该用低浓度的多肽以避免多肽的低聚反应。头尾相连式合成环状多肽的产率取决于链状多肽的序列。因此,在大规模制备环状多肽前,首先应该创建可能的链状先导多肽库,然后进行环化以寻找能达到结果的序列。
2、糖基化
我们最常见的糖肽如万古霉素和替考拉宁,是治疗耐药细菌感染的重要抗生素,其他糖肽常被用于刺激免疫系统。另外,由于很多微生物抗原是糖基化的,因此研究糖肽对提高感染的治疗效果具有重要意义。另一方面,有研究发现肿瘤细胞细胞膜上的蛋白质表现出异常的糖基化,这使得糖肽在癌症和肿瘤免疫防御研究中也发挥着重要作用。糖肽的制备一般利用Fmoc/t-Bu方法。糖基化残基,比如苏氨酸和丝氨酸常通过五氟苯酚酯活化的Fmoc保护糖基化氨基酸引入到多肽中。
3、磷酸化
在人类细胞中,超过30%的蛋白质被磷酸化。磷酸化,尤其是可逆磷酸化,在控制许多细胞过程中起重要作用,如信号转导、基因表达、细胞周期和细胞骨架调节以及细胞凋亡。
磷酸化可以在各种氨基酸残基上观察到,但最常见的磷酸化目标是丝氨酸、苏氨酸和酪氨酸残基。磷酸酪氨酸、磷酸苏氨酸和磷酸丝氨酸衍生物既可在合成中引入到多肽也可在多肽合成以后形成。使用可选择性移除保护基团的丝氨酸、苏氨酸和酪氨酸残基可以实现选择性磷酸化。一些磷酰化试剂也可通过后修饰在多肽中引入磷酸基团。最近,也有学者使用化学选择性的Staudinger-亚磷酸酯反应实现了赖氨酸的位点特异性磷酸化的案例。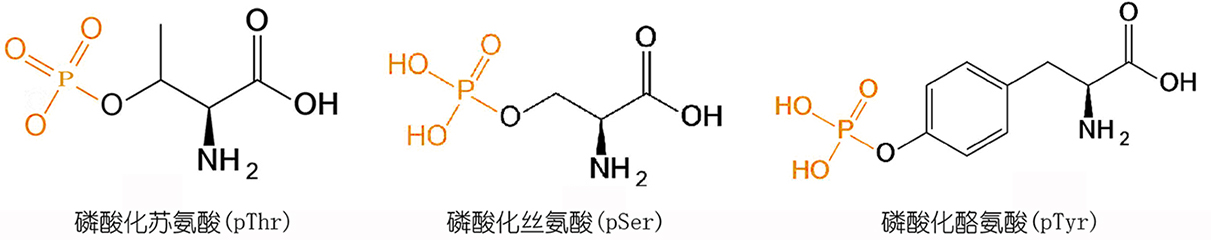
4、N-甲基化
N-甲基化通常被用来引入到多肽合成中以阻止氢键的形成,进而使得多肽更加耐受生物降解和清除,最初出现在天然多肽中。利用N-甲基化的氨基酸衍生物(如Fmoc-N-Me-Val-OH,Fmoc-N-Me-Trp(Boc)-OH等)合成多肽是最主要的方法,另外也可利用N-(2-硝基苯磺酰氯)多肽-树脂中间体与甲醇进行Mitsunobu反应,该方法已被用于制备含有N-甲基化氨基酸的环状多肽库。
5、豆蔻酰化和棕榈酰化
通过多肽N末端脂肪酸酰化可以让多肽或蛋白质与细胞膜结合。N末端上豆蔻酰化的多肽可以使Src家族的蛋白激酶和逆转录酶Gaq蛋白靶向结合细胞膜。利用标准的酰胺缩合反应即可将豆蔻酸连接到树脂-多肽的N末端,生成的脂肽可在标准条件下解离并通过RP-HPLC纯化。
6、生物素化
生物素可以与亲和素或者链霉亲和素有力结合,结合强度甚至接近共价键。生物素标记的肽通常用于免疫测定,组织细胞化学和基于荧光的流式细胞术。标记的抗生物素抗体也可以用来结合生物素化多肽。生物素标记常连接在赖氨酸侧链或者N末端。通常在多肽和生物素之间使用6-氨基己酸作为纽带,纽带能够灵活结合底物,并且在有空间位阻的情况下能结合地更好。
7、荧光标记
人们利用利用荧光标记的多肽来检测目标蛋白的活性,并将其发展的高通量活性筛选方法应用于疾病治疗靶点蛋白的药物筛选和药物开发(例如,各种激酶、磷酸酶、肽酶等)。常用的荧光剂有FITC, FAM, TAMRA, CY3, CY5, Rhodamine等。色氨酸(Trp)也带有荧光,因此可以被用于内在标记。色氨酸的发射光谱取决于外围环境,随着溶剂极性降低而降低,这种性质对于检测多肽结构和受体结合很有用处。色氨酸荧光可以被质子化的门冬氨酸和谷氨酸淬灭,这可能会限制其使用。丹磺酰氯基团(Dansyl)与氨基结合时具有高度荧光,也常被用于氨基酸或蛋白质的荧光标记。
荧光共振能量转换(FRET)对酶的研究十分有用,应用FRET时,底物多肽常含有一个荧光标记基团和一个荧光淬灭基团。标记的荧光基团会被淬灭剂通过非光子能量传递淬灭。当多肽从所研究的酶上解离下来,标记基团就会发射荧光。
8、聚乙二醇(PEG)修饰
PEG修饰可用于改善蛋白水解稳定性、生物分布和肽的溶解度。在多肽上引入PEG链可以改善它们的药理性质,也可以抑制多肽被蛋白水解酶水解。PEG多肽比普通多肽更容易通过肾小球毛细血管截面,大大减少肾清除率。由于PEG多肽在体内的有效半衰期延长,因此使用更低剂量、更低频度的多肽药物便可以维持正常治疗水平。但PEG修饰也存在负效应。大量PEG在阻止酶降解多肽的同时也会减少多肽与目标受体的结合。但PEG多肽的低亲和力通常被其更长的药动学半衰期抵消,通过在体内存在更久,PEG多肽有更大可能性被目标组织吸收。因此,PEG聚合物的规格应该针对结果进行化设计。另一方面,由于肾清除率降低,PEG多肽会在肝脏累积造成大分子综合征。因此,当多肽用于药物测试时需要更加谨慎地设计PEG修饰。
PEG修饰剂常见的修饰基团大致可总结如下:氨基(-Amine)-NH2,氨甲基-CH2-NH2,羟基-OH,羧基-COOH,巯基(-Thiol)-SH,马来酰亚胺-MAL,琥珀酰亚胺碳酸酯-SC,琥珀酰亚胺乙酸酯-SCM,琥珀酰亚胺丙酸酯-SPA,N-羟基琥珀酰亚胺-NHS,丙酸基-CH2CH2COOH,醛基-CHO(如丙醛-ALD,丁醛-butyrALD),丙烯酸基(-Acrylate)-ACRL,叠氮基-Azide,生物素基-Biotin,荧光素基-Fluorescein,戊二酸基-GA,酰肼基-Hydrazide,炔基-Alkyne,对甲苯磺酸酯基-OTs,琥珀酰亚胺琥珀酸酯-SS等。带有羧酸的PEG衍生物可以与N末端的胺或者赖氨酸侧链进行偶联。氨基活化的PEG可以与门冬氨酸或者谷氨酸侧链偶联。MAL活化的PEG可以与完全脱保护的半胱氨酸侧链的硫醇进行偶联。PEG修饰剂常见分类如下(注:mPEG即methoxy-PEG,CH3O-(CH2CH2O)n-CH2CH2-OH):
(1)直链PEG修饰剂
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2)双官能团PEG修饰剂
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3)分枝形PEG修饰剂
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
9、多聚抗原肽(MAP)
短肽通常不具有免疫性,必须和载体蛋白耦合才能产生抗体。多聚抗原肽(MAP)由多个连接到赖氨酸核的相同多肽构成,能特异性表达高效免疫原,可用来制备肽-载体蛋白耦联体。MAP多肽可以在MAP树脂上利用固相合成法分步合成。然而,不完整的耦合会在一些分支上产生遗失或截断肽链,因而表现不出原本MAP多肽的性质。作为替代性的方法,多肽可以单独制备和纯化然后再耦联到MAP上。连接到多肽核心上的多肽序列是明确的,并且很容易通过质谱表征。
10、异戊二烯化
异戊二烯化发生在C末端附近侧链上的半胱氨酸残基。蛋白质的异戊二烯化可以提高细胞膜亲和性,形成蛋白质-蛋白质相互作用。异戊二烯化的蛋白质包括酪氨酸磷酸酶、小GTP酶、协同伴侣分子、核纤层和着丝粒结合蛋白。异戊二烯化的多肽可以利用树脂上的异戊二烯化方法或者引入半胱氨酸衍生物制备。
结语:
多肽修饰是一种设计多肽的重要手段,经过化学修饰的多肽不仅可以维持较高的生物活性, 而且能够有效地避免免疫原性和毒性方面的缺点,同时化学修饰可以赋予多肽一些新的优良性能。肽谷生物经常长期不断的摸索与创新,在多肽修饰方面积累的大量宝贵经验,同时也为广大科研工作者提供了大量的高品质修饰多肽与优良的售前收货服务,肽谷生物竭诚欢迎您的咨询!