·研究在试管环境中测试了7种药物对新型冠状病毒的抗性,其中瑞德西韦和氯喹能有效抑制病毒。
·瑞德西韦是美国制药公司吉利德正在研发的药物,目前由中日友好医院在武汉牵头,与制药公司合作,已经投入临床试验。
·氯喹的使用已有逾75年历史,是原用于治疗痢疾的药物,是一种廉价和安全的药物。
Cell Research杂志在线发表了来自中国科学院武汉病毒研究所、生物安全大科学研究中心肖庚富,胡志红及军事医学科学院毒物药物研究所钟武共同通讯的论文。论文中表示,在体外试验中,发现瑞德西韦(Remdesivi)和氯喹(chloroquine)能有效抑制新型冠状病毒。
寻找“解药”的有效方式,就是测试现有的抗病毒药物能否有效治疗新的病毒,研究中使用了7种常见的抗病毒相关药物,其中有5种是经过FAD批准的药物——利巴韦林(ribavirin)、潘昔洛韦(penciclovir)、硝唑尼特( nitazoxanide,)、萘莫司他(nafamostat)、氯喹(chloroquine),另外还有两种注明的广谱抗病毒药物瑞德西韦(remdesivir,GS-5734) 和法匹拉韦( favipiravir),来测试出他们对临床分离的新型冠状病毒的细胞毒性。
研究发现在Vero E6细胞上,瑞德西韦(Remdesivir, GS-5734)和氯喹(Chloroquine)在细胞水平上能有效抑制新型冠状病毒的感染,其在人体上的作用还有待临床药物。其他的5种药物对抗新型冠状病毒的感染都不太理想。
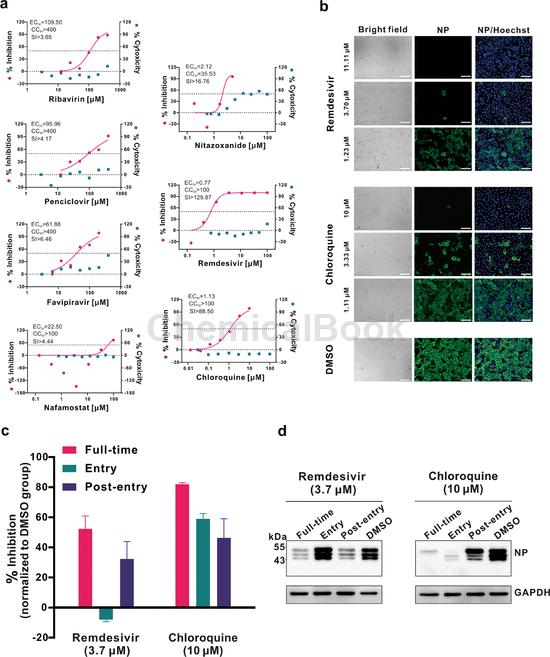
体外实验证实瑞德西韦和氯喹可抑制新型冠状病毒
瑞德西韦(Remdesivir)是美国制药公司吉利德正在研发的药物,它本是针对埃博拉病毒进行研发的。在美国首例病患的诊疗过程中,它在患者情况恶化是被临床应用,随后患者迅速好转。
氯喹则是一种原用于治疗疟疾的药物,在临床应用上已经有超过75年的历史。氯喹除了具有抗病毒活性外,还具有免疫调节活性,这可能会协同增强其在体内的抗病毒作用。氯喹经口服后广泛分布于全身,包括肺,是一种廉价和安全的药物。
2019年12月,拥有一千一百万人口的中国中部城市武汉,出现了一种由先前未知的病原体引起的新型肺炎。最初的病例与武汉市海鲜市场的暴露有关。截至2020年1月27日,中国当局报告在中国大陆确诊2835例病例,包括81例死亡。此外,在香港,澳门和台湾发现了19例确诊病例,在泰国,日本,韩国,美国,越南,新加坡,尼泊尔,法国,澳大利亚和加拿大发现了39例输入病例。该病原体很快被鉴定为新型冠状病毒(2019-nCoV),与严重急性呼吸系统综合症冠状病毒(SARS-CoV)密切相关。目前,尚无针对这种新病毒的特异性治疗方法。因此,迫切需要找到有效的抗病毒药物来对抗这种疾病。
一种有效药物的发现方法是测试现有的抗病毒药物是否能有效治疗相关病毒感染。2019-nCoV属于乙型冠状病毒,也包含SARS-CoV和中东呼吸综合征CoV(MERS-CoV)。 SARS或MERS患者使用了几种药物,例如利巴韦林,干扰素,洛匹那韦-利托那韦,皮质类固醇,尽管有些药物的疗效尚存争议。在这项研究中,我们评估了五种FAD批准药物的抗病毒功效包括利巴韦林,潘昔洛韦,硝唑尼特,萘莫司他,氯喹和两种针对2019-nCoV临床分离株的广谱抗病毒药物瑞德昔韦(GS5734)和法维拉韦(T-705)。
研究人员进行了标准测定以测量这些化合物对2019-nCoV的细胞毒性、病毒产量和感染率的影响。首先,通过CCK8分析确定候选化合物在Vero E6细胞(ATCC-1586)中的细胞毒性。然后,在不同浓度的测试药物存在下,用nCoV——2019BetaCoV / Wuhan / WIV04 / 20192感染Vero E6细胞,感染复数(MOI)为0.05。在对照中使用DMSO。通过定量实时RT-PCR(qRT-PCR)测定细胞上清液中的病毒拷贝数来评估功效,并在感染后(pi)48小时通过免疫荧光显微镜通过可视化病毒核蛋白(NP)的表达进行确认(细在感染的这个时间点并未观察到细胞病变)。在这7种受试药物中,高浓度的三种核苷类似物包括利巴韦林(半有效浓度(EC50)= 109.50μM,半细胞毒性浓度(CC50)> 400μM,选择性指数(SI)> 3.65),潘昔洛韦(EC50 = 95.96 μM,CC50> 400μM,SI> 4.17)和法匹拉韦(EC50 = 61.88μM,CC50> 400μM,SI> 6.46)才能减少病毒感染(图1a和补充信息,图S1)。然而,法匹拉韦已显示出100%的有效保护小鼠抵抗埃博拉病毒的攻击,尽管在Vero E6细胞中的EC50值高达67μM,表明可以进行进一步的体内研究以评估这种抗病毒核苷。 萘莫司他(是一种有效的MERS-CoV抑制剂,可防止膜融合,可抑制2019-nCoV感染(EC50 = 22.50μM,CC50> 100μM,SI> 4.44)。硝唑尼特(Nitazoxanide)是一种具有商业潜力的原生动物药物,具有针对包括人和动物冠状病毒在内的多种病毒的抗病毒潜力,可在低微摩尔浓度下抑制2019-nCoV(EC50 = 2.12μM; CC50> 35.53μM; SI> 16.76)。建议对该药物针对2019-nCoV感染进行进一步的体内评估。值得注意的是,两种化合物瑞德昔韦(EC50 = 0.77μM; CC50> 100μM; SI> 129.87)和氯喹(EC50 = 1.13μM; CC50> 100μM,SI> 88.50)在低微摩尔浓度下有效地阻断了病毒感染并显示出高SI值(图1a,b)。
瑞德昔韦最近被公认为是针对培养细胞,小鼠和非人类灵长类动物(NHP)模型中的多种RNA病毒(包括SARS / MERS-CoV5)感染的有前途的抗病毒药物。目前正在临床研究中,用于治疗埃博拉病毒感染。瑞德昔韦是一种腺苷类似物,可整合到新生的病毒RNA链中并导致过早终止。我们的加药时间分析显示瑞德昔韦在病毒进入后的一个阶段起作用(图1c,d),这与其作为核苷酸类似物的推定抗病毒机制是一致的。沃伦等的结果表明,在NHP模型中,静脉内施用10 mg / kg剂量的瑞德昔韦可导致其活性形式在血液中持续存在(10μM),并提供100%的抗埃博拉病毒感染保护作用。我们的数据表明瑞德昔韦在Vero E6细胞中针对2019-nCoV的EC90值为1.76μM,这表明在NHP中可能达到其工作浓度。我们的初步数据(补充信息,图S2)表明,瑞德昔韦还可以有效抑制人细胞系(人肝癌Huh-7细胞)中的病毒感染,该细胞系对2019-nCoV.2敏感。
氯喹是一种广泛使用的抗疟疾和自身免疫性疾病药物,最近被报道为潜在的广谱抗病毒药物。8氯喹通过增加病毒/细胞融合所需的内体pH值以及干扰来阻断病毒感染,同时也能干扰SARS-CoV受体的糖基化反应。我们的添加时间分析表明,氯喹在Vero E6细胞中2019-nCoV感染的进入和进入后阶段均起作用(图1c,d)。除了其抗病毒活性外,氯喹还具有免疫调节能力,可在体内协同增强其抗病毒作用。口服后,氯喹广泛分布于整个身体,包括肺。氯喹对Vero E6细胞中2019-nCoV的EC90值为6.90μM,这在风湿性关节炎患者接受500毫克给药的血浆中可证明是临床上可实现的。氯喹是一种便宜且安全的药物使用了70多年,因此,它可能在临床上适用于2019-nCoV。
我们的发现表明,瑞德昔韦和氯喹在体外控制2019-nCoV感染方面非常有效。由于这些化合物已用于人类患者,并具有安全跟踪记录,还显示出对各种疾病的有效效果,因此我们建议应在患有新型冠状病毒疾病的人类患者中对它们进行评估。
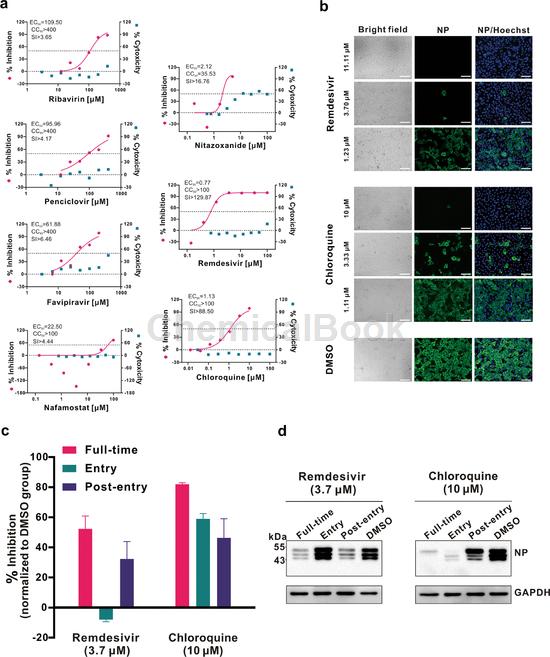
体外实验证实瑞德西韦和氯喹可抑制新型冠状病毒
测试药物在体外对2019-nCoV的抗病毒活性。在不同剂量的所示抗病毒药物治疗中,将Vero E6细胞以MOI为0.05水平的2019-nCoV进行感染,持续48小时。然后通过qRT-PCR测定细胞上清液中的病毒产量。通过CCK-8测定法测量了这些药物对Vero E6细胞的细胞毒性。图a的左和右Y轴分别代表对病毒产量的抑制和药物的细胞毒性的平均%。实验一式三份进行。 图b为使用瑞姆昔韦和氯喹后病毒感染的免疫荧光显微镜检查。如上所述药物治疗有效。感染后48 h,固定感染的细胞,然后用兔血清针对蝙蝠SARS相关CoV的NP作为一抗,并用Alexa 488标记的山羊抗兔IgG(1:500; Abcam)作为二抗。细胞核用赫斯特染料染色。条为100μm。 图c和d为瑞地昔韦和氯喹的添加时间实验。对于“全过程治疗”,将Vero E6细胞用药物预处理1小时,然后添加病毒使其附着2小时。之后,去除病毒和药物的混合物,并用含药物的培养基培养细胞,直到实验结束。对于“进入治疗”,在病毒附着前将药物添加到细胞中1小时,然后在p.i. 2 h,将病毒-药物混合物替换为新鲜培养基,并保持到实验结束。对于“进入后”实验,药物在p.i. 2 h加入,并保持到实验结束。对于所有实验组,将细胞用2019-nCoV感染,MOI为0.05,并通过qRT-PCR c测量感染细胞上清液中的病毒产量,并在14 h p.i时通过Western blot d分析感染细胞中的NP表达。
通讯作者:中国科学院武汉病毒研究所/生物安全大科学研究中心肖庚富、胡志红及军事医学科学院毒物药物研究所钟武
发布日期:2020年2月4日
发布渠道:Cell Research
原文地址:https://www.nature.com/articles/s41422-020-0282-0
原文标题:Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro
