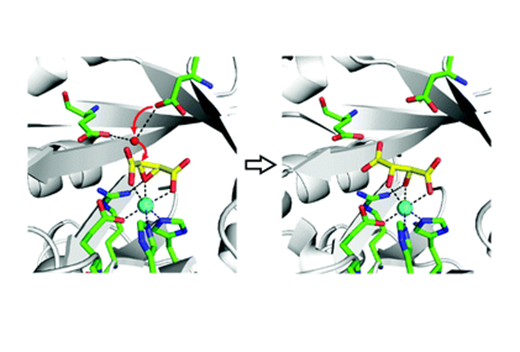
中国科学院青岛生物能源与过程研究所代谢物组学研究组研究人员在前期获得的CESH[D]高纯度表达纯化的基础上,通过与清华大学研究人员合作,成功解析了CESH[D]的高分辨晶体结构,并根据结构阐释了CESH[D]的立体催化机制,发表在Chem. Commun.上[1]。CESH[D]的结构表明,一个锌离子在底物结合中起到了关键作用,而周边残基通过大量的氢键作用使得催化残基和底物被精确固定,从而实现了高精度的立体催化,产生高对映体纯度的D-酒石酸。对CESH[D]的结构和催化机制的阐明,同时为基于这类酶进行新型生物催化剂设计开发提供了基础。
参考文献
[1] Structural insight into the catalytic mechanism of a cis-epoxysuccinate hydrolase producing enantiomerically pure d(−)-tartaric acid. doi: 10.1039/C8CC04398A
