背景及概述[1][2]
白桦脂酸(分子结构见图1, BA) 是一种五环三萜类化合物,在天然界中广泛存在,最早分离于生长在非洲东部的鼠李科常绿植物的树皮,但主要来源是从白桦树皮中提取纯化。近年科学研究发现,BA是非常有价值的天然产物。BA 及其衍生物作为生物制剂在抗癌和 HIV治疗等方面表现出了巨大的潜能,在机体的抗氧化损伤和免疫调节过程中发挥着重要作用,是一类很有潜力的药物先导化合物,对于新药的研发具有重要价值,美国癌症研究所NCI已将其列入快速研发规划项目(RAID)。但该化合物在白桦树皮中的含量很低,大约只含有0.025%,长期采伐已导致白桦树资源的严重短缺,更是严重影响着BA的开发利用。
制备[1]
1 天然提取法
BA不仅存在于白桦树皮中,也存在于蒲桃树、酸枣仁、悬铃木、大枣等多种植物中。天然提取法即不经过化学合成的过程,采用不同的溶剂将BA 从不同的植物中提取出来。Liu等优化选择绿色环保高产的亚临界水萃取(SWE) 提取方法,得到了产率为2.803 mg /g 的BA。天然提取法虽然方法简单,但是BA 在植物中的含量很少,因此对原料的消耗极大,杂质较多,产率低下,直接从植物中提取BA 还没有潜在的工业化价值,往往只是作为提取桦木醇的一种副产物。
2 一步合成法
一步合成法是将桦木醇的提取和 BA 的制备同步进行,采用二氯甲烷、 氯仿、丙酮、四氢呋喃、DMF等有机溶剂浸提植物,提取含量较高的桦木醇,同时将硝酸锌、硝酸铬等氧化剂附着在硅胶、 氧化铝、 胶岭石等固相载体上,将提取的桦木醇氧化,得到 BA。这种方法由于提取到的桦木醇没有进行分离纯化就直接进行氧化,得到的产物成分复杂,杂质多,因此实际应用价值不大。
3 半合成法
半合成法是从植物中先提取出桦木醇,然后由桦木醇经过一系列化学反应制得 BA。桦木醇在植物中的含量相对较高,目前其获得途径主要通过直接提取,且提取成本相对较低,因此以其为原料合成BA 能降低成本,具有良好的工业化前景。Melnikova N 等通过以氧化铝为载体在水丙酮( 15~25℃)溶液中Cr(VI) 化合物的催化,桦木醇能够选择性的氧化为BA,不仅得到了93%~98%的收益率,也通过氧化铝吸附去除了毒性的反应混合物,提供了一个简单和友好环境的反应。
4 微生物转化法
微生物转化法是利用生物在代谢过程中产生的酶对底物催化反应得到目标产物。与化学合成方法相比,微生物转化具有高立体选择性、反应条件温和、污染小、费用低,这种方法具有工业化的潜力。Feng 等通过培养 Armillaria luteovirens ZJUQH100-6、Cunninghamella blakesleeana 细胞催化桦木醇直接微生物转化产生 BA。另外,有研究首次利用 Ocimum 物种愈伤组织诱导生产 BA 的生物技术,提高了BA的产率,该研究为BA以及其他抗癌三萜烯等的制备提供了新的方法。近来,有研究报道将植物中BA的整个代谢通路代入酵母细胞, 成功地利用微生物合成了BA。研究发现脂肪酸和萜类前体合成途径的代谢流平衡对 BA 合成影响显著,并通过协同表达这两个代谢通路中的关键调控基因( HFA1、HMG1 和ERG9) 显著提高BA产量,该工程菌每升培养基能合成毫克级的 BA,由此,BA 的制备合成上升到了一个新的高度。
药理作用[2]
1 抗肿瘤活性
最早的研究报道是BA对黑色素瘤细胞具有极强的选择性细胞毒性,IC50 值为0.5~4.8mg /mL,更重要的是,这项研究也显示BA的体内疗效,对裸鼠皮下注射黑色素瘤细胞株 MEL-2, 腹腔注射50、250 或500mg/kg BA 产生高效的肿瘤生长抑制,宿主细胞没有任何毒性的迹象。
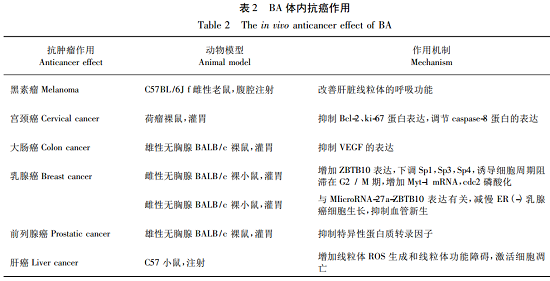
Leopoldo C等对BA对肿瘤细胞的选择性进行了研究,发现其对肿瘤细胞的选择性毒性很高, 约是正常细胞的5~7 倍。近年来发现 BA 对其它肿瘤细胞也有较为广谱的活性作用,如对胶质母细胞瘤,神经母细胞瘤,成神经管细胞瘤,尤因肿瘤以及其他恶性肿瘤,结肠癌、乳腺癌、肺癌、肝癌、前列腺癌、肾细胞、卵巢或子宫颈癌和白血病等均有较强的抑制作用。除了其在各种癌症细胞系强大的抗肿瘤活性,也有研究表明 BA 能抑制动物体内肿瘤生长(表2)。
2抗 HIV 活性
BA 最突出的生物活性之一就是具有抗病毒活性,尤其是具有抗艾滋病毒(HIV) 活性。由于HIV耐药株出现以及长期药物治疗所带来的副作用, 使得治疗 AIDS 更加困难。目前,从天然产物中寻找和发现活性成分,并将其作为先导物,进行结构修饰改造,是新型抗 HIV 药物研究与开发的重要策略。对 BA 进行衍生化研究优化抗艾滋病活性,个被报道表现出极大抗艾滋病活性的 BA 衍生品为RPR103611,被认为是融合抑制剂的个低分子量化合物,该化合物在对抗 HIV-1 的体外实验中发现IC50值介于 40 至 100 nmol/L之间, 能防止HIV-1感染的细胞和未感染的CD4细胞之间合胞体形成,通过抑制依赖外壳粘合的病毒感染达到抗HIV-1 作用。
目前公认的抗艾滋病的作用机制是抑制 HIV-1逆转录酶或抑制蛋白酶的活性,由于BA 衍生物的结构与己知抗逆转录药物的结构完全没有联系,其作用机理也不同于临床现有的酶抑制剂。基于多位点修饰改造及构效关系研究,发现大量 BA 高活性衍生品比一些当前临床抗艾滋病药物表现出更好的治疗指数,更强大的抗 HIV 作用,可认为它是一类很有前途的抗 HIV-l 候选化合物,但其作用机制尚未完全确定。
主要参考资料
[1]周亚敏,林丽美,夏伯候.白桦脂酸制备方法和药理活性研究进展[J].天然产物研究与开发,2016,28(06):978-985.
